Table of Contents
5
अम्ल, क्षारक और लवण

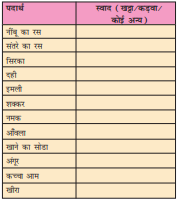
अपने दैनिक जीवन में हम नींबू, इमली, नमक, शक्कर और सिरके जैसे अनेक पदार्थों का उपयोग करते हैं। क्या इन सबका स्वाद एक समान होता है? आइए, हम सारणी 5.1 में सूचीबद्ध किए
गए कुछ खाद्य पदार्थों के स्वाद पर ध्यान दें। यदि आपने इनमें से किसी भी पदार्थ का स्वाद नहीं चखा हो, तो उसे चखिए और परिणामों को सारणी 5.1
में लिखिए।
आप देखेंगे कि इनमें से कुछ पदार्थों का स्वाद खट्टा, कुछ का कड़वा, कुछ का मीठा और कुछ का नमकीन है।


5.1 अम्ल और क्षारक
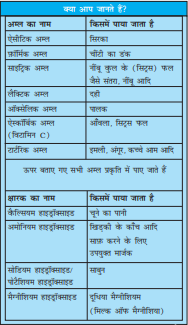
दही, नींबू का रस, संतरे का रस और सिरके का स्वाद खट्टा होता है। इन पदार्थों का स्वाद खट्टा इसलिए होता है, क्योंकि इनमें अम्ल (एसिड) होते हैं। एेसे पदार्थों की रासायनिक प्रकृति अम्लीय होती है। एसिड शब्द की उत्पत्ति लैटिन शब्द एसियर से हुई है, जिसका अर्थ है खट्टा। इन पदार्थों में पाए जाने वाले अम्ल प्राकृतिक अम्ल होते हैं।
खाने का सोडा (बेकिंग सोडा) कैसा होता है? क्या इसका स्वाद भी खट्टा है? यदि नहीं, तो इसका स्वाद कैसा है? क्योंकि इसका स्वाद खट्टा नहीं है, जिसका मतलब है, इसमें कोई अम्ल नहीं है। इसका स्वाद कड़वा है। यदि आप इसके विलयन को अपनी अँगुलियों के बीच रगड़ें, तो यह साबुन जैसा चिकना लगता है। सामान्यतः एेसे पदार्थ, जिनका स्वाद कड़वा होता है और जो स्पर्श करने पर साबुन जैसे लगते हैं, क्षारक कहलाते हैं। इन पदार्थों की प्रकृति क्षारकीय कहलाती है।
यदि हम किसी पदार्थ को चख नहीं सकते हैं, तो हमें उसकी प्रकृति कैसे ज्ञात होगी?
कोई पदार्थ अम्लीय है अथवा क्षारकीय, इसका परीक्षण करने के लिए विशेष प्रकार के पदार्थों का उपयोग किया जाता है। ये पदार्थ सूचक कहलाते हैं। सूचकों को जब अम्लीय अथवा क्षारकीय पदार्थयुक्त विलयन में मिलाया जाता है, तो उनका रंग बदल जाता है। हल्दी, लिटमस, गुड़हल की पंखुड़ियाँ आदि कुछ प्राकृतिक रूप से पाए जाने वाले सूचक हैं।
5.2 हमारे आस-पास के प्राकृतिक सूचक
लिटमसः एक प्राकृतिक रंजक
सबसे सामान्य रूप से उपयोग किया जाने वाला प्राकृतिक सूचक लिटमस है। इसे लाइकेनों (शैक) से निष्कर्षित किया जाता है (चित्र 5.1a)। आसुत जल में इसका रंग मॉव (नीलशोण) होता है। जब इसे अम्लीय विलयन में मिलाया जाता है, तो यह लाल हो जाता है और जब क्षारीय विलयन में मिलाया जाता है, तो यह नीला हो जाता है। यह विलयन के रूप में अथवा कागज़ की पट्टियों के रूप में उपलब्ध होता है, जिन्हें लिटमस पत्र कहते हैं। सामान्यतः यह लाल और नीले लिटमस पत्र के रूप में उपलब्ध होता है (चित्र 5.1b)।



(b)
चित्र 5.1 (a) लाइकेन और (b) लाल व नीला लिटमस पत्र
क्रियाकलाप 5.1
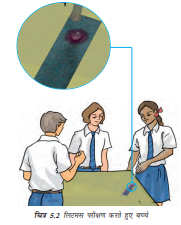
- इसी परीक्षण को नीले लिटमस पत्र के साथ दोहराइए।
नोट कीजिए कि क्या रंग में कोई परिवर्तन हो रहा है?
इसी क्रियाकलाप को निम्नलिखित पदार्थों के साथ दोहराइएः
नलके का पानी, अपमार्जक (डिटर्जेंट) का घोल, वातित पेय पदार्थ, साबुन का विलयन, शैम्पू, सामान्य नमक का विलयन, शक्कर का विलयन, सिरका, बेकिंग सोडे का विलयन, दूधिया मैग्नीशियम, धावन सोडे का विलयन तथा चूने का पानी (यदि संभव हो, तो विलयन आसुत जल में बनाएँ)।
चूने का पानी बनाने के लिए किसी बोतल में चूने की कुछ मात्रा पानी में घोलिए। विलयन को भली-भाँति हिलाकर कुछ देर रखा रहने दीजिए। अब बोतल के ऊपरी भाग से कुछ द्रव को किसी बर्तन में निथार लीजिए। यह द्रव ही चूने का पानी है।
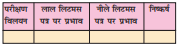
अपने प्रेक्षणों को सारणी 5.2 में नोट कीजिए।
सारणी 5.2
क्या आपकी सूची में कुछ एेसे विलयन हैं, जिनका लिटमस पत्र पर कोई प्रभाव नहीं होता? इन पदार्थों के नाम लिखिए।
एेसे विलयन, जो लाल अथवा नीले लिटमस पत्र के रंग को परिवर्तित नहीं करते, उदासीन विलयन कहलाते हैं। एेसे पदार्थ न तो अम्लीय होते हैं और न ही क्षारकीय।
हल्दी एक अन्य प्राकृतिक सूचक है
क्रियाकलाप 5.2
- एक चम्मच हल्दी पाउडर लीजिए। इसमें थोड़ा जल मिलाकर इसका पेस्ट बनाइए।
- स्याही सोख्ता (ब्लॉटिंग पेपर) या फ़िल्टर पत्र पर हल्दी का पेस्ट लगाकर हल्दी पत्र बनाइए और उसे सुखा लीजिए। हल्दी पत्र की पतली-पतली पट्टियाँ काट लीजिए।
- हल्दी पत्र की पट्टी पर एक बूँद साबुन का विलयन डालिए।
आप क्या देखते हैं?
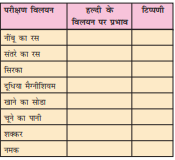
इसी प्रकार सारणी 5.3 में दिए गए विलयनों का परीक्षण कीजिए, और अपने प्रेक्षणों को सारणी 5.3 में नोट कीजिए। आप अन्य पदार्थों के विलयनों से भी परीक्षण कर सकते हैं।
सारणी 5.3
आप अपनी माताजी के जन्मदिन पर, उनके लिए विशेष बधाई पत्र बना सकते हैं। सादे सफेद कागज़ की शीट पर हल्दी का पेस्ट लगाइए और उसे सुखा लीजिए। रुई के फाहे की सहायता से इस पर चूने के पानी से एक खूबसूरत फूल बनाइए। आपको एक सुंदर बधाई पत्र मिल जाएगा।

हल्दी का पेस्ट चूने का पानी
सूचक के रूप में गुड़हल के पुष्प
क्रियाकलाप 5.3
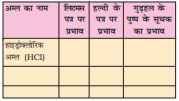
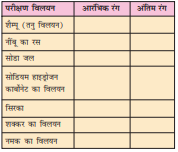
गुड़हल के पुष्प की कुछ पंखुड़ियाँ एकत्र कीजिए और उन्हें किसी बीकर में रख दीजिए। इसमें थोड़ा गरम जल मिलाइए। मिश्रण को कुछ समय तक रखिए, जब तक जल रंगीन न हो जाए। रंगीन जल को सूचक के रूप में उपयोग कीजिए। इस सूचक की पाँच-पाँच बूँदें सारणी 5.4 में दिए गए प्रत्येक विलयन में मिलाइए।
सारणी 5.4
सूचक का अम्लीय, क्षारकीय और उदासीन विलयनों पर क्या प्रभाव पड़ता है? गुड़हल के पुष्प का सूचक अम्लीय विलयनों को गहरा गुलाबी (मेजेन्टा)
और क्षारकीय विलयनों को हरा कर देता है
(चित्र 5.3)।
अब मैं समझ गया कि मेरी सफ़ेद कमीज़ पर पड़ा हल्दी का दाग साबुन से धोने पर लाल क्यों हो जाता है। एेसा इसलिए होता है, क्योंकि साबुन का विलयन क्षारकीय होता है।
जब मैं शुष्क लिटमस पत्र खाने के सोडे के ठोस कण रखता हूँ, तो मुझे सही परिणाम नहीं मिलते। क्यों?![boojho_02]()
खाने के सोडे का विलयन बनाकर परीक्षण करो।![paheli_1]()
चित्र 5.3 गुड़हल का पुष्प और उससे तैयार किया गया सूचक
आप इन प्राकृतिक सूचकों को बनाकर उनसे अम्लीय, क्षारकीय और उदासीन विलयनों में रंग परिवर्तन देखने का प्रयास कर सकते हैं।
पहेली आपके लिए निम्नलिखित समस्या लेकर आई है।
कॉफ़ी का रंग है भूरा
और स्वाद है कड़वा
अम्ल है यह, या है क्षार
प्रश्न बड़ा ही है दुश्वार
स्वाद के कारण से अनजान
बिना परीक्षण हो ना ज्ञान
क्रियाकलाप 5.4
शिक्षक/शिक्षिका से अपेक्षित है कि वे अपने विद्यालय की प्रयोगशाला अथवा आस-पास के किसी विद्यालय से निम्नलिखित रसायनों के तनु विलयन लें। हाइड्रोक्लोरिक अम्ल, सल्फ्यूरिक अम्ल, नाइट्रिक अम्ल, एेसीटिक अम्ल, सोडियम हाइड्रॉक्साइड, अमोनियम हाइड्रॉक्साइड तथा कैल्सियम हाइड्रॉक्साइड (चूने का पानी)। इनमें से प्रत्येक विलयन पर तीनों सूचकों के प्रभाव को प्रदर्शित कीजिए। अपने प्रेक्षणों को सारणी 5.5 में लिखिए।
चेतावनी
प्रयोगशाला अम्लों और क्षारकों के रखरखाव तथा उपयोग में अत्यधिक सावधानी बरतनी चाहिए, क्योंकि ये संक्षारक प्रकृति के होते हैं, जो त्वचा में जलन उत्पन्न करते हैं और उसे हानि पहुँचाते हैं।
5.3 उदासीनीकरण
हमने पढ़ा है कि अम्ल नीले लिटमस को लाल कर देते हैं और क्षारक लाल लिटमस को नीला कर देते हैं। आइए, अब यह देखें कि जब किसी अम्ल को किसी क्षारक में मिलाया जाता है, तो क्या होता है?
हम उस सूचक का उपयोग करने जा रहे हैं, जिसका आपने अभी तक उपयोग नहीं किया है। इसे फ़िनॉल्फथेलिन कहते हैं।
क्रियाकलाप 5.5
(यह क्रियाकलाप शिक्षक द्वारा कक्षा में निदर्शित किया जाना चाहिए।)
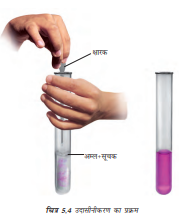
किसी परखनली के एक-चौथाई भाग को तनु हाइड्रोक्लोरिक अम्ल से भर लीजिए। इसका रंग नोट कीजिए। फ़िनॉल्फथेलिन विलयन के रंग को भी नोट कीजिए। सूचक के 2-3 बूँद अम्ल में मिलाइए
(चित्र 5.4)। परखनली को धीरे-धीरे हिलाइए।
क्या आपको अम्ल के रंग में कोई परिवर्तन दिखाई देता है?
अम्लीय विलयन में ड्रॉपर से सोडियम हाइड्रॉक्साइड की एक बूँद डालिए। परखनली को धीरे-धीरे हिलाइए। क्या विलयन के रंग में कोई परिवर्तन होता है? विलयन को निरंतर हिलाते हुए बूँद-बूँद करके सोडियम हाइड्रॉक्साइड विलयन डालना तब तक जारी रखिए, जब तक कि हल्का गुलाबी रंग न आ जाए।
अब इसमें तनु हाइड्रोक्लोरिक अम्ल की एक बूँद और मिलाइए। आप क्या देखते हैं? क्या विलयन पुनः रंगहीन हो जाता है? फिर से सोडियम हाइड्रॉक्साइड की एक बूँद मिलाइए। क्या रंग में कोई परिवर्तन होता है? विलयन पुनः गुलाबी हो जाता है।
यह स्पष्ट है कि जब विलयन क्षारकीय होता है, तो फ़िनॉल्फथेलिन गुलाबी रंग देता है। इसके विपरीत, जब विलयन अम्लीय होता है, तो यह रंगहीन रहता है।
जब किसी अम्लीय विलयन में क्षारकीय विलयन मिलाया जाता है तो दोनों विलयन एक दूसरे के प्रभाव को उदासीन कर देते हैं। जब किसी अम्ल और क्षारक के विलयन को उचित मात्रा में मिलाया जाता है,
तो विलयन की प्रकृति न तो अम्लीय रहती है और न ही क्षारकीय। दूसरे शब्दों में, अम्ल तथा क्षारक दोनों की ही प्रकृति लुप्त हो जाती हैं। इस प्रकार बना विलयन न तो अम्लीय होता है और न ही क्षारकीय। उदासीनीकरण के तत्काल बाद परखनली को स्पर्श करें। आपने क्या अनुभव किया? उदासीनीकरण अभिक्रिया में सदैव ऊष्मा निकलती है, अर्थात् निर्मुक्त होती है। निर्मुक्त ऊष्मा से अभिक्रिया मिश्रण का ताप बढ़ जाता है।
उदासीनीकरण अभिक्रिया में नया पदार्थ निर्मित होता है, जो लवण कहलाता है। लवण अम्लीय, क्षारकीय अथवा उदासीन प्रकृति का हो सकता है। अतः उदासीनीकरण को निम्न रूप में परिभाषित किया जा सकता हैः
किसी अम्ल और किसी क्षारक के बीच होने वाली अभिक्रिया उदासीनीकरण कहलाती है। इस प्रक्रम में ऊष्मा के निर्मुक्त होने के साथ-साथ लवण और जल निर्मित होते हैं।
क्या आप अम्ल वर्षा शब्द से परिचित हैं? क्या आपने कभी अम्ल वर्षा के क्षतिकारी प्रभावों के बारे में सुना है? जैसा कि नाम से पता चलता है, जब वर्षा जल में अम्ल की मात्रा अत्यधिक होती है, तो वह अम्ल वर्षा कहलाती है। वर्षा जल में ये अम्ल कहाँ से आते हैं? वर्षा जल, अम्लीय इसलिए हो जाता है, क्योंकि कार्बन डाइअॉक्साइड, सल्फ़र डाइअॉक्साइड और नाइट्रोजन डाइअॉक्साइड जैसी गैसें (जो वायु में प्रदूषकों के रूप में निर्मुक्त होती है) वर्षा जल में घुलकर क्रमशः कार्बोनिक अम्ल, सल्फ़्यूरिक अम्ल और नाइट्रिक अम्ल बनाती हैं। अम्ल वर्षा, भवनों, एेतिहासिक इमारतों, पौधों और जंतुओं को क्षति पहुँचा सकती है।
अम्ल + क्षारक → लवण + जल
(ऊष्मा निर्मुक्त होती है)
निम्नलिखित अभिक्रिया इसका उदाहरण हैः
हाइड्रोक्लोरिक अम्ल (HCl) + सोडियम हाइड्रॉक्साइड (NaOH) → सोडियम क्लोराइड (NaCl)
+ जल (H2O) + (ऊष्मा)
बूझो ने चूने के पानी में तनु सल्फ्यूरिक अम्ल मिलाया। अभिक्रिया मिश्रण गर्म हो जाएगा अथवा ठंडा?
5.4 दैनिक जीवन में उदासीनीकरण के उदाहरण
अपाचन
हमारे आमाशय में हाइड्रोक्लोरिक अम्ल पाया जाता है। आप अध्याय 2 में पढ़ चुके हैं कि यह भोजन के पाचन में हमारी सहायता करता है, लेकिन आमाशय में अम्ल की आवश्यकता से अधिक मात्रा होने से अपाचन हो जाता है। कभी-कभी अपाचन काफी कष्टदायक होता है। अपाचन से मुक्ति पाने के लिए हम दूधिया मैग्नीशियम जैसा कोई प्रतिअम्ल लेते हैं जिसमें मैग्नीशियम हाइड्रॉक्साइड होता है। यह अत्यधिक अम्ल के प्रभाव को उदासीन कर देता है।
चींटी का डंक
जब चींटी काटती है तो यह त्वचा में अम्लीय द्रव डाल देती है। डंक के प्रभाव को नमीयुक्त खाने का सोडा (सोडियम हाइड्रोजनकार्बोनेट) अथवा कैलेमाइन विलयन मलकर उदासीन किया जा सकता है, जिसमें जिंक कार्बोनेट होता है।
मृदा उपचार
रासायनिक उर्वरकों का अत्यधिक उपयोग मृदा को अम्लीय बना देता है। यदि मृदा अत्यधिक अम्लीय अथवा अत्यधिक क्षारकीय हो, तो पादपों (पौधाें) की वृद्धि अच्छी नहीं होती। जब मृदा अत्यधिक अम्लीय होती है, तो उसे बिना बुझा हुआ चूना (कैल्सियम अॉक्साइड) अथवा बुझा हुआ चूना (कैल्सियम हाइड्रॉक्साइड) जैसे क्षारकों से उपचारित किया जाता है। यदि मृदा क्षारकीय हो, तो इसमें जैव पदार्थ मिलाए जाते हैं। जैव पदार्थ (कम्पोस्ट खाद्) मृदा में अम्ल निर्मुक्त करते हैं, जो उसकी क्षारकीय प्रकृति को उदासीन कर देते हैं।
कारखानों का अपशिष्ट
अनेक कारखानों के अपशिष्ट (कचरे) में अम्लीय पदार्थ मिश्रित होते हैं। यदि एेसे अपशिष्ट पदार्थों को सीधे ही जलाशयों व नदियों में बहने दिया (विसर्जित किया) जाए, तो मछली और अन्य जलीय जीवों को अम्ल नष्ट कर सकते हैं। अतः कारखाने के अपशिष्ट को जलाशयों व नदियों में विसर्जित करने से पहले क्षारकीय पदार्थ मिलाकर उदासीन किया जाता है।
प्रमुख शब्द
अम्ल
क्षारक
सूचक
उदासीन विलयन
उदासीनीकरण
लवण
आपने क्या सीखा
- अम्ल स्वाद में खट्टे होते हैं। सामान्यतः क्षारकों का स्वाद कड़वा होता है तथा उनका स्पर्श साबुन जैसा होता है।
- अम्ल नीले लिटमस को लाल कर देते हैं। क्षारक लाल लिटमस को नीला कर देते हैं।
- वे पदार्थ, जो न तो अम्लीय होते हैं और न ही क्षारकीय, उदासीन कहलाते हैं।
- एेसे पदार्थों के विलयन, जो अम्लीय, क्षारकीय और उदासीन विलयन में भिन्न रंग दर्शाते हैं, सूचक कहलाते हैं।
- अम्ल और क्षारक एक-दूसरे को उदासीन करके लवण बनाते हैं। लवण अम्लीय, क्षारकीय अथवा उदासीन प्रकृति के होते हैं।
अभ्यास
1. अम्लों और क्षारकों के बीच अंतर बताइए।
2. अनेक घरेलू उत्पादों, जैसे खिड़की साफ़ करने के मार्जकों आदि में अमोनिया पाया जाता है। ये लाल लिटमस को नीला कर देते हैं। इनकी प्रकृति क्या है?
3. उस स्रोत का नाम बताइए, जिससे लिटमस विलयन को प्राप्त किया जाता है। इस विलयन का क्या उपयोग है?
4. क्या आसुत जल अम्लीय/क्षारकीय/उदासीन होता है? आप इसकी पुष्टि कैसे करेंगे।
5. उदासीनीकरण के प्रक्रम को एक उदाहरण देते हुए समझाइए।
6. निम्नलिखित कथन यदि सही हैं, तो (T) अथवा गलत हैं, तो (F) लिखिए।
(क) नाइट्रिक अम्ल लाल लिटमस को नीला कर देता है।
(ख) सोडियम हाइड्रॉक्साइड नीले लिटमस को लाल कर देता है।
(ग) सोडियम हाइड्रॉक्साइड और हाइड्रोक्लोरिक अम्ल एक-दूसरे को उदासीन करके लवण और जल बनाते हैं।
(घ) सूचक वह पदार्थ है, जो अम्लीय और क्षारकीय विलयनों में भिन्न रंग दिखाता है।
(च) दंत क्षय, क्षार की उपस्थिति के कारण होता है।
7. दोरजी के रैस्टोरेन्ट में शीतल (मृदु) पेय की कुछ बोतलें हैं। लेकिन दुर्भाग्य से वे चिह्नित नहीं हैं। उसे ग्राहकों की माँग के अनुसार पेय परोसने हैं। एक ग्राहक अम्लीय पेय चाहता है, दूसरा क्षारकीय और तीसरा उदासीन पेय चाहता है। दोरजी यह कैसे तय करेगा, कि कौन-सी बोतल किस ग्राहक को देनी है।
8. समझाइए, एेसा क्यों होता हैः
(क) जब आप अतिअम्लता से पीड़ित होते हैं, तो प्रतिअम्ल की गोली लेते हैं।
(ख) जब चींटी काटती है, तो त्वचा पर कैलेमाइन का विलयन लगाया जाता है।
(ग) कारखाने के अपशिष्ट को जलाशयों में बहाने से पहले उसे उदासीन किया जाता है।
9. आपको तीन द्रव दिए गए हैं, जिनमें से एक हाइड्रोक्लोरिक अम्ल है, दूसरा सोडियम हाइड्रॉक्साइड और तीसरा शक्कर का विलयन है। आप हल्दी को सूचक के रूप में उपयोग करके उनकी पहचान कैसे करेंगे?
10. नीले लिटमस पत्र को एक विलयन में डुबोया गया। यह नीला ही रहता है। विलयन की प्रकृति क्या है? समझाइए।
11. निम्नलिखित वक्तव्यों को ध्यान से पढ़ेंः
(क) अम्ल और क्षारक दोनों सभी सूचकों के रंगों को परिवर्तित कर देते हैं।
(ख) यदि कोई सूचक अम्ल के साथ रंग परिवर्तित कर देता है, तो वह क्षारक के साथ रंग परिवर्तन नहीं करता।
(ग) यदि कोई सूचक क्षारक के साथ रंग परिवर्तित करता है, तो वह अम्ल के साथ रंग परिवर्तन नहीं करता।
(घ) अम्ल और क्षारक में रंग परिवर्तन सूचक के प्रकार पर निर्भर करता है।
ऊपर लिखे वक्तव्यों में से कौन-से वक्तव्य सही हैं?
(i) सभी चार
(ii) (क) और (घ)
(iii) (ख) (ग) और (घ)
(iv) केवल (घ)
विस्तारित अधिगम-क्रियाकलाप और परियोजना कार्य
1. अम्लों और क्षारकों के ज्ञान का उपयोग करते हुए, खाने के सोडे और चुकंदर की सहायता से एक गुप्त संदेश लिखिए। समझाइए यह कैसे कार्य करता है।
(संकेतः जल में खाने के सोडे का विलयन बनाइए। इस विलयन का उपयोग सफ़ेद कागज़ की शीट पर रुई के फाहे से संदेश लिखने के लिए कीजिए। संदेश के सूख जाने के बाद उस पर ताजी कटी चुकंदर का एक टुकड़ा मलिए।)
2. लाल पत्तागोभी के टुकड़ों को जल में उबालकर उसका रस तैयार कीजिए। इसका उपयोग सूचक के रूप में करके इससे अम्लीय और क्षारकीय विलयनों का परीक्षण कीजिए। अपने प्रेक्षणों को एक सारणी में प्रस्तुत कीजिए।
3. अपने क्षेत्र की मृदा का एक नमूना लीजिए। यह मालूम कीजिए, कि यह अम्लीय है, क्षारकीय है अथवा उदासीन। किसानों के साथ बातचीत कीजिए कि वे मृदा का उपचार किस प्रकार करते हैं।
4. किसी चिकित्सक से यह जानने का प्रयास कीजिए, कि अतिअम्लता का उपचार करने के लिए वे कौन-सी औषधि लेने का सुझाव देते हैं। उनसे यह जानने का प्रयास कीजिए, कि अतिअम्लता से कैसे बचा जा सकता है।
क्या आप जानते हैं?
हमारे शरीर की प्रत्येक कोशिका में एक अम्ल, डी-अॉक्सीराइबोन्यूक्लीइक अम्ल अथवा DNA होता है। यह शरीर के अनेक व्यक्तिगत गुणों, जैसे हमारे रंग-रूप, आँखों के रंग, ऊँचाई आदि का निर्धारण करता है। सभी प्रोटीन, जो कि हमारी कोशिकाओं के भाग होते हैं, भी एमीनो अम्लों के बने होते हैं। हमारे शरीर में पाई जाने वाली वसा, वसा अम्ल होते हैं।