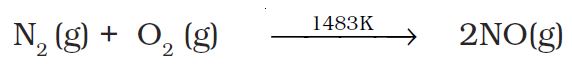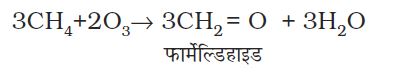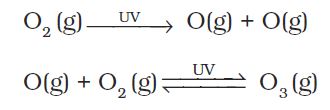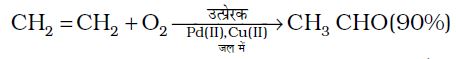Table of Contents
एकक 14
पर्यावरणीय रसायन
Environmental Chemistry
विश्व ने ज्ञानरहित चमक तथा विवेकहीन शक्ति प्राप्त कर ली है। हमारा विश्व नाभिकीय रूप से महादानव तथा नैतिक रूप से शिशु है।
उद्देश्य
इस एकक के अध्ययन के बाद आप–
• पर्यावरणीय रसायन का अर्थ समझ सकेंगे;
• वायुमंडलीय प्रदूषण को परिभाषित कर सकेंगे तथा भूमंडलीय तापवृद्धि, हरित गृह-प्रभाव तथा अम्ल-वर्षा के कारणों की सूची बना सकेंगे;
• ओजोन-परत के अवक्षय के कारणों तथा इसके प्रभावों को जान सकेंगे;
• जल-प्रदूषण के कारण बता सकेंगे तथा पेयजल के अंतरराष्ट्रीय मानकों के बारे में जान सकेंगे;
• मृदा-प्रदूषण के कारणों की व्याख्या कर सकेंगे;
• पर्यावरणीय प्रदूषण की रोकथाम के लिए योजना बना और अपना सकेंगे;
• दैनिक जीवन में हरित रसायन के महत्त्व को समझ सकेंगे।
पिछली कक्षाओं में आप पर्यावरण के बारे में अध्ययन कर चुके हैं। पर्यावरणीय अध्ययन परिवेश से हमारे सामाजिक, जैविक, आर्थिक, भौतिक तथा रासायनिक अंतर्संबंध को दर्शाता है। इस एकक में हम पर्यावरणीय रसायन पर ध्यान केंद्रित करेंगे। पर्यावरणीय रसायन परिवहन, अभिक्रियाओं, प्रभावोें, तथ्यों आदि पर्यावरणीय रासायनिक स्पीशीज़ से संबंधित हैं। आइए, पर्यावरणीय रसायन के कुछ महत्त्वपूर्ण पहलुओं पर विचार करें।
14-1 पर्यावरण-प्रदूषण
पर्यावरण-प्रदूषण हमारे परिवेश में अवांछनीय परिवर्तन (जो पौधों, जंतुओं तथा मनुष्यों पर हानिकारक प्रभाव डालते हैं) का परिणाम है। वह पदार्थ, जो प्रदूषण उत्पन्न करता है, ‘प्रदूषक’ कहलाता है। प्रदूषक ठोस, द्रव अथवा गैसीय पदार्थ हो सकता है, जो प्राकृतिक घटनाओं के कारण उत्पन्न होता है। क्या आप जानते हैें कि एक औसत मनुष्य को भोजन की तुलना में लगभग 12-15 गुना अधिक वायु की आवश्यकता होती है? अतः भोजन में प्रदूषक की अति अल्प मात्रा वायु में उपस्थित समान मात्रा की तुलना में महत्त्वपूर्ण है। प्रदूषक को निम्नीकृत किया जा सकता है। उदाहरणार्थ– सब्जियों के त्याज्य भाग प्राकृतिक विधियों द्वारा निम्नीकृत एवं अपघटित हो जाते हैं। इसके विपरीत कुछ प्रदूषक, जो धीरे-धीरे निम्नीकृत होते हैं, कई दशकों तक पर्यावरण में अपरिवर्तित रूप में बने रहते हैं। उदाहरणार्थ– डाइक्लोरोडाइफिनाइल ट्राइक्लोरो एथेन (डी.डी.टी.), प्लास्टिक-निर्मित अनेक पदार्थ, भारी धातुएँ, अनेक रसायन तथा नाभिकीय अपशिष्ट आदि यदि एक बार पर्यावरण में निर्गमित हो जाते हैं, तो इन्हें पृथक् करना कठिन होता है। ये प्रदूषक प्राकृतिक विधियों द्वारा निम्नीकृत नहीं होते हैं तथा जीवित प्राणियों के लिए हानिकारक होते हैं। पर्यावरणीय प्रदूषण में प्रदूषक विभिन्न स्रोतों से उत्पन्न होते हैं तथा वायु या जल मनुष्य द्वारा अथवा मृदा में गाड़ने पर अभिगमित होते हैं।
14-2 वायुमंडलीय प्रदूषण
वायुमंडल, जो पृथ्वी को चारों ओर से घेरे हुए है, की मोटाई हर ऊँचाई पर समान नहीं होती है। इसमें वायु की विभिन्न संकेंद्री परत अथवा क्षेत्र होते हैं तथा प्रत्येक परत का घनत्व भिन्न-भिन्न होता है। वायुमंडल का सबसे निचला क्षेत्र, जिसमें मनुष्य तथा अन्य प्राणी रहते हैं, को ‘क्षोभमंडल’ (Troposphere) कहते हैं। यह समुद्र-तल से 10 किमी. की ऊँचाई तक होता है। उसके ऊपर (समुद्र-तल से 10 से 50 किमी. के मध्य) समतापमंडल (Stratosphere) होता है। क्षोभमंडल धूलकणों से युक्त क्षेत्र है, जिसमें वायु, अधिक जलवाष्प तथा बादल उपस्थित होते हैं। इस क्षेत्र में वायु के तीव्र प्रवाह एवं बादल का निर्माण होता है, जबकि समतापमंडल में डाइनाइट्रोजन, डाइअॉक्सीजन, ओजोन तथा सूक्ष्म मात्रा में जलवाष्प होता है।
वायुमंडलीय प्रदूषण में मुख्यतः क्षोभमंडलीय तथा समतापमंडलीय प्रदूषण का अध्ययन किया जाता है। सूर्य की हानिकारक पराबैगनी किरणों के 99.5% भाग को समतापमंडल में उपस्थित ओजोन पृथ्वी की सतह पर पहुँचने से रोकता है तथा इसके प्रभाव मानव तथा अन्य जीवों की रक्षा करता है।
14-2-1 क्षोभमंडलीय प्रदूषण
वायु में उपस्थित अवांछनीय ठोस अथवा गैस कणों के कारण क्षोभमंडलीय प्रदूषण होता है। क्षोभमंडल में निम्नलिखित मुख्यतः गैसीय तथा कणिकीय प्रदूषक उपस्थित होते हैं–
(क) गैसीय वायुप्रदूषक– ये सल्फर, नाइट्रोजन तथा कार्बन के अॉक्साइड, हाइड्रोजन सल्फाइड, हाइड्रोकार्बन, ओजोन तथा अन्य अॉक्सीकारक हैं।
(ख) कणिकीय प्रदूषक- ये धूल, धूम्र, कोहरा, फुहारा (स्प्रे), धुआँ आदि हैं।
1. गैसीय वायुप्रदूषक–
(d) सल्फर के अॉक्साइड– जीवाश्म ईंधन के दहन के परिणामस्वरूप सल्फर के अॉक्साइड उत्पन्न होते हैं। इसमें प्रमुख स्पीशीज़ सल्फर डाइअॉक्साइड है। यह एक गैस है तथा मनुष्य एवं जंतुओं के लिए विषैली है। एेसा प्रतीत होता है कि सल्फर डाइअॉक्साइड की सूक्ष्म सांद्रता मनुष्य में विभिन्न श्वसन-रोगों (जैसे–अस्थमा, श्वसनी शोध (Bronchities), एेम्फाइसीमा आदि) का कारण होती है। सल्फर डाइअॉक्साइड के कारण आँखों में जलन होती है, जिससे आँखें लाल हो जाती हैं तथा आँसू आने लगते हैं। SO2 की उच्च सांद्रता फूलों की कलियों में कड़ापन उत्पन्न करती है, जिससे ये पौधों से शीघ्र गिर जाती हैं। सल्फर डाइअॉक्साइड का अनुत्प्रेरकीय (Uncatalysis) अॉक्सीकरण एक धीमी प्रक्रिया है, परंतु प्रदूषित वायु, जिसमें कणिकीय द्रव्य होते हैं, वायुमंडल में उपस्थित सल्फर ट्राइअॉक्साइड की अॉक्सीकरण-प्रक्रिया को उत्प्रेरित करते हैं।
2SO2 (g) +O2 (g) → 2SO3(g)
इस अभिक्रिया की प्रगति वायुमंडल में उपस्थित ओजोन तथा हाइड्रोजन परॉक्साइड द्वारा बढ़ जाती है।
SO2 (g) + O3 (g) → SO3(g) + O2 (g)
SO2(g) + H2O2(l) → H2SO4(aq)
(ख) नाइट्रोजन के अॉक्साइड– वायु के प्रमुख अवयव डाइनाइट्रोजन तथा डाइअॉक्सीजन हैं। सामान्य ताप पर ये गैसें आपस में अभिक्रिया नहीं करती हैं, परंतु उच्च उन्नतांश पर जब बिजली चमकती है, तब ये आपस में प्रतिक्रिया करके नाइट्रोजन के अॉक्साइड बनाती हैं। NO2 अॉक्सीकरण पर NO–3 आयन बनाती है, जो मृदा में घुलकर उर्वरक का कार्य करती है। किसी स्वचालित इंजन में (उच्च ताप पर) जब जीवाश्म ईंधन का दहन होता है, तब डाइनाइट्रोजन तथा डाइअॉक्सीजन मिलकर नाइट्रिक अॉक्साइड NO तथा नाइट्रोजन डाइअॉक्साइड NO2 की पर्याप्त मात्रा देती हैं।
NO अॉक्सीजन से शीघ्रतापूर्वक क्रिया कर NO2 देती है।
2NO (g) + O2 (g) → 2NO2 (g)
जब समतापमंडल में नाइट्रिक अॉक्साइड NO ओजोन से प्रतिक्रिया करती है, तब नाइट्रोजन डाइअॉक्साइड (NO2) के निर्माण की दर बढ़ जाती है।
NO (g) + O3 (g) → NO2 (g) + O2 (g)
यातायात तथा सघन स्थानों पर उत्पन्न तीक्ष्ण लाल धूम्र नाइट्रोजन अॉक्साइड के कारण होता है। NO2 की अधिक सांद्रता होने पर पौधों की पत्तियाँ गिर जाती हैं तथा प्रकाश-संश्लेषण की दर कम हो जाती है। नाइट्रोजन डाइअॉक्साइड फेफड़ों में उत्तेजना उत्पन्न होती है, जिससे बच्चों में प्रचंड श्वसन-रोग उत्पन्न हो जाते हैं। यह जीव ऊतकों के लिए विषैली भी है। नाइट्रोजन डाइअॉक्साइड विभिन्न वस्त्र-रेशों तथा धातुओं के लिए भी हानिकारक है।
(ग) हाइड्रोकार्बन– हाइड्रोकार्बन केवल कार्बन तथा हाइड्रोजन के बने होते हैं। स्वचालित वाहनों में ईंधन के अपूर्ण दहन के कारण ये उत्पन्न होते हैं। अधिकांश हाइड्रोकार्बन कैन्सरजन्य होते हैं, अर्थात् इसके कारण कैन्सर होता है। यह पौधों में काल-प्रभावण, ऊतकों के निम्नीकरण तथा पत्तियों, फूलों एवं टहनियों में छाया द्वारा हानि पहुँचाते हैं।
(घ) कार्बन के अॉक्साइड
(i) कार्बन मोनोअॉक्साइड– कार्बन मोनो अॉक्साइड गंभीर वायु-प्रदूषकाें में से एक है। यह रंगहीन तथा गंधहीन है। यह श्वसनीय प्राणियों के लिए हानिकारक है। इसमें विभिन्न अंगों तथा ऊतकों के लिए दी जाने वाली अॉक्सीजन के प्रवाह को रोकने की सामर्थ्य होती है। यह कार्बन के अपूर्ण दहन के फलस्वरूप उत्पन्न होती है। इसकी सर्वाधिक मात्रा मोटरवाहनों से निकलने वाले धुएँ से उत्पन्न होती है। इसके अन्य स्रोत कोयला, ईंधन-लकड़ी, पेट्रोल का अपूर्ण दहन हैं। विश्व में पिछले कुछ वर्षों में यातायात के साधनों की संख्या में तेजी से वृद्धि हुई है। अधिकतर वाहनों का उचित रख-रखाव नहीं होता है अथवा प्रदूषक, नियंत्रक उपकरण उपयुक्त नहीं होते हैैं। परिणामस्वरूप अत्यधिक मात्रा में कार्बन मोनोअॉक्साइड तथा अन्य प्रदूषक गैसें निर्गमित होती हैं। क्या आप जानते हैं कि कार्बन मोनोअॉक्साइड विषैली क्यों है? यह हीमोग्लोबिन के साथ अॉक्सीजन की अपेक्षा अधिक प्रबलता से संयुक्त हो जाती है तथा कार्बोक्सी हीमोग्लोबिन बनाती है, जो अॉक्सीजन-होमोग्लोबिन से लगभग 300 गुना अधिक स्थायी संकुल है। जब रक्त में कार्बोक्सीहीमोग्लोबिन की मात्रा 3-4 प्रतिशत तक पहुँच जाती है, तब रक्त में अॉक्सीजन ले जाने की क्षमता काफी कम हो जाती है। अॉक्सीजन की इस न्यूनता से सिरदर्द, नेत्रदृष्टि की क्षीणता, तंत्रकीय आवेग में न्यूनता, हृदयवाहिका में तंत्र अव्यवस्था आदि की विसंगतियाँ हो जाती हैं। यही कारण है कि लोगों को धूम्रपान नहीं करने की सलाह दी जाती है। गर्भवती महिलाआें के रक्त में कार्बन मोनोअॉक्साइड CO की बढ़ी मात्रा कालपूर्व जन्म, स्वतः गर्भपात एवं बच्चों में विरूपता का कारण है। यह इतनी विषैली है कि 1300 पी.पी.एम. की सांद्रता आधे घंटे में प्राणघातक हो जाती है।
(ii) कार्बन डाइअॉक्साइड– श्वसन, जीवाश्म ईंधन का दहन, सीमेन्ट निर्माण में काम आने वाले चूना-पत्थर आदि से वायुमंडल में कार्बन डाइअॉक्साइड (CO2) निर्गमित होती है। कार्बन डाइअॉक्साइड गैस केवल क्षोभमंडल में होती है। सामान्यतः वायुमंडल में इसकी मात्रा आयतन के अनुसार 0.03% होती है। जीवाश्म ईंधन के अधिक प्रयोग से वायुमंडल में कार्बन डाइअॉक्साइड की अधिक मात्रा निर्गमित होती है। कार्बन डाइअॉक्साइड की अधिकता हरित पौधों द्वारा कम कर दी जाती है, जिससे वायुमंडल में CO2 की यथेष्ट मात्रा बनी रहती है। वातावरण में CO2 की मात्रा बनाए रखना आवश्यक होता है। हरे पौधों में प्रकाश-संश्लेषण के लिए CO2 की आवश्यकता होती है। फलतः अॉक्सीजन मुक्त होती है। इसलिए संतुलित चक्र बना रहता हैै। जैसा आप जानते हैं, वनों के कटने तथा जीवाश्म ईंधन के अधिक दहन के कारण वायुमंडल में CO2 की मात्रा बढ़ गई है तथा पर्यावरण-संतुलन बिगड़ गया है। कार्बन डाइअॉक्साइड की यही बढ़ी हुई मात्रा भूमंडलीय तापवृद्धि के लिए उत्तरदायी है।
भूमंडलीय तापवृद्धि एवं हरितगृह प्रभाव (Global Warming and Greenhouse Effect)
सौर ऊर्जा का 75% भाग पृथ्वी की सतह द्वारा अवशोषित कर लिया जाता है, जिससे इसके ताप में वृद्धि होती है। शेष ऊष्मा वायुमंडल में पुनः विकिरित हो जाती है। ऊष्मा का कुछ भाग वायुमंडल में उपस्थित गैसों (जैसे–कार्बन डाइअॉक्साइड, ओजोन, क्लोरोफ्लोरो कार्बन यौगिकों तथा जलवाष्प) द्वारा प्रग्रहित कर लिया जाता है, जिससे वायुमंडल के ताप में वृद्धि होती है। यही भूमंडलीय तापवृद्धि का कारण है।
हम जानते हैं कि ठंडे स्थानों पर फूल, सब्जियाँ, फल आदि काँच-आवरण क्षेत्र (जिसे ‘हरितगृह’ कहते हैं) में विकसित होते हैं। क्या आप जानते हैं कि हम मनुष्य भी हरितगृह में रहते हैं? यद्यपि हम किसी काँच द्वारा आवरित नहीं रहते हैं, तथापि वायु का एक आवरण, जिसे ‘वायुमंडल’ कहते हैं, शताब्दियों से पृथ्वी का ताप स्थिर रखे हुए हैं, परंतु आजकल इसमें धीमा परिवर्तन हो रहा है। जिस प्रकार हरितगृह में काँच सूर्य की गरमी को अंदर थामे रखता है, उसी प्रकार वायुमंडल सूर्य की ऊष्मा को पृथ्वी के निकट अवशोषित कर लेता है तथा इसे गरम बनाए रखता हैै। इसे ‘प्राकृतिक हरितगृह प्रभाव’ कहते हैं, क्योंकि यह पृथ्वी के तापमान की रक्षा करके जीवन-योग्य बनाता है। दृश्यप्रकाश हरितगृह में पारदर्शी काँच में से गुजरकर सूर्य के विकिरण मृदा तथा पौधों को गरम रखते हैं। गरम मृदा तथा पौधे उष्मीय क्षेत्र के अवरक्त विकिरणाें का उत्सर्जन करते हैं। चूँकि इस विकिरण के लिए काँच अपारदर्शक होता है, अतः यह इन विकिरणों को आंशिक रूप से अवशोषित तथा शेष को परावर्तित करता है। यह क्रियाविधि सौर-ऊर्जा को हरितगृह में संग्रहीत रखती है। इसी प्रकार कार्बन डाइअॉक्साइड के अणु ऊष्मा को संग्रहीत कर लेते हैं, क्योंकि ये सूर्य के प्रकाश के लिए पारदर्शक होते हैं, ऊष्मा विकिरणों के लिए नहीं। यदि कार्बन डाइअॉक्साइड की मात्रा 0.03% से अधिक हो जाती है, तो प्राकृतिक हरितगृह का संतुलन बिगड़ जाता है। भूमंडलीय तापवृद्धि में कार्बन डाइअॉक्साइड का विशिष्ट योगदान है।
कार्बन डाइअॉक्साइड के अतिरिक्त अन्य हरितगृह गैसें, मेथैन (CH4), जलवाष्प, नाइट्रसअॉक्साइड (N2O), क्लोरो- फ्लोरोकार्बन तथा ओजोन हैं। अॉक्सीजन की अनुपस्थिति में जब वनस्पतियों को जलाया, पचाया अथवा सड़ाया जाता है, तब मेथैन उत्पन्न होती है। धान के क्षेत्रों, कोयले की खानों, दलदली क्षेत्रों तथा जीवाश्म ईंधनों द्वारा अधिक मात्रा में मेथैन उत्पन्न होती है। क्लोरोफ्लोरोकार्बन मनुष्य द्वारा निर्मित रसायन है, जो वायुप्रशीतक आदि में काम आता है। क्लोरोफ्लोरोकार्बन भी ओजोन-परत को हानि पहुँचा रहे हैं (खंड 14.2.2)। नाइट्रस अॉक्साइड (N2O) वातावरण में प्राकृतिक रूप से उत्पन्न होता है, परंतु पिछले कुछ वर्षों में जीवाश्म ईंधन एवं उर्वरकों के अधिक प्रयोग से इसकी मात्रा में उल्लेखनीय वृद्धि हुई है। यदि इसी प्रकार तापवृद्धि का क्रम बना रहा, तो ध्रुवों पर स्थित हिमनदों के पिघलने की दर अधिक होगी, जिससे समुद्र के जल-स्तर में वृद्धि के फलस्वरूप पृथ्वी के निचले स्थानों में जल भर जाएगा। भूमंडलीय तापवृद्धि के कारण बहुत से संक्रामक रोगों, जैसे–डेंगू, मलेरिया, पीत ज्वर, निद्रा रोग आदि में वृद्धि होती है।
अम्लवर्षा (Acid rain)
हम जानते हैं कि वायुमंडल में उपस्थित कार्बन डाइअॉक्साइड द्वारा जल से की गई अभिक्रिया के फलस्वरूप उत्पन्न H+ आयन के कारण वर्षाजल की pH सामान्यतः 5.6 होती है–
H2O (l) + CO2 (g) → H2CO3 (aq)
H2CO3 (aq) → H +(aq) + (aq)
जब वर्षा की pH 5.6 से कम हो जाती है, तो इसे ‘अम्लवर्षा’ कहते हैं।
‘अम्लवर्षा’ में वायुमंडल से पृथ्वी-सतह पर अम्ल निक्षेपित हो जाता है। अम्लीय प्रकृति के नाइट्रोजन एवं सल्फर के अॉक्साइड वायुमंडल में ठोस कणों के साथ हवा में बहकर या तो ठोस रूप में अथवा जल में द्रव रूप में कुहासे से या हिम की भाँति निक्षेपित होते हैं (चित्र 14.1)।
पुनः विचार करें
भूमंडलीय तापवृद्धि को कम करने के लिए हम क्या कर सकते हैं? चूँकि जीवाश्म ईंधन को जलाने तथा वनों को काटने से वायुमंडल में हरितगृह गैसों में वृद्धि हो रही है, अतः इसके सुचारु, बुद्धिमत्ता एवं न्यायपूर्ण उपयोग के उपाय हमें तलाशने होंगे, जो भूमंडलीय तापवृद्धि को कम करने में सहायक हों। इसका एक साधारण उपाय परिस्थितियों को ध्यान में रखकर यातायात के व्यक्तिगत साधनों का कम प्रयोग साइकिल को प्रोत्साहन देना तथा जनसाधारण के यातायात-साधनों को काम से लेना अथवा कारपूल का प्रयोग आदि है। अधिक पौधे लगाकर हरित-आवरण को बढ़ाने का प्रयास हमें करना चाहिए। शुष्क पत्तियों, लकड़ी आदि को नहीं जलाना चाहिए। जनसाधारण के कार्यस्थलों पर धूम्रपान करना गैर-कानूनी है। चूँकि यह केवल धूम्रपान करने वाले व्यक्ति के लिए ही नहीं, अपितु आस-पास खड़े अन्य व्यक्तियों के लिए भी हानिकारक होता है। अतः हमें इसे त्यागना चाहिए। अनेक व्यक्ति हरित गृहप्रभाव तथा भूमंडलीय तापवृद्धि के बारे में नहीं जानते हैं। उन्हें इस तथ्य से अवगत कराना चाहिए।
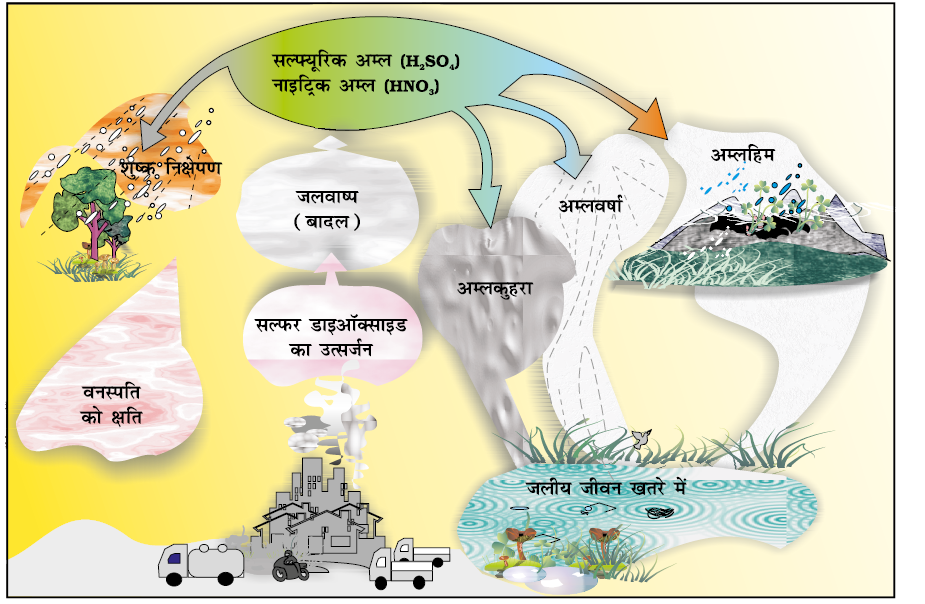
चित्र 14.1 अम्ल-निक्षेपण
अम्लवर्षा मानवीय क्रियाकलापों का उपोत्पाद होती है,जो वातावरण में नाइट्रोजन तथा सल्फर के ऑक्साइड निर्गमित करती है। जैसा पूर्व में बताया जा चुका है, जीवाश्म-ईंधन(जैसे- कोयला, शक्ति-संयंत्रें, भट्टियों तथा मोटर इंजनों में डीजल और पेट्रोल, (जिसमें सल्फर तथा नाइट्रोजन पदार्थ होते हैं) के दहन पर सल्फर डाइऑक्साइड तथा नाइट्रोजन ऑक्साइड उत्पन्न होते हैं। SO2 तथा NO2 ऑक्सीकरण के पश्चात् जल के साथ अभिक्रिया करके अम्लवर्षा में प्रमुख योगदान देते हैं, क्योंकि प्रदूषित वायु में सामान्यतः कणिकीय द्रव्य उपस्थित होते हैं, जो ऑक्सीकरण को उत्प्रेरित करते हैं।
2SO2 (g) + O2 (g) + 2H2O (l) → 2H2SO4 (aq)
4NO2 (g) + O2 (g)+ 2H2O (l) → 4HNO3 (aq)
इसमें अमोनियम लवणों का भी निर्माण होता है, जो वायुमंडलीय धुंध (एरॉसॉल के सूक्ष्म कण) के रूप में दृश्यमान होते हैं। वर्षा की बूँदों में ऑक्साइड तथा अमोनियम लवणों के एरोसॉल कण के फलस्वरूप नम विक्षेपण (Wet Deposition) होता है। ठोस तथा द्रव भूमि-सतहों द्वारा SO2 सीधे अवशोषित हो जाते हैं। इस प्रकार शुष्क निक्षेपण (Dry Deposition) होता हैै।
अम्लवर्षा कृषि, पेड़-पौधों आदि के लिए हानिकारक होती है, क्योंकि यह इनकी वृद्धि के लिए आवश्यक पोषक तत्वों को घोलकर पृथव्फ़ कर देती है। यह मनुष्यों तथा जानवरों में श्वसन-अवरोध उत्पन्न करती है। जब यह सतही जल के साथ बहकर नदी एवं झीलों तक पहुँचती है, तो जलीय परिस्थितियों के पौधों एवं जंतुओं के जीवन को प्रभावित करती है। अम्लवर्षा के कारण जल के पाइपों का संक्षारण होता है, जिससे आयरन, लेड, कॉपर आदि धातुएँ घुलकर पेयजल में पहुँच जाती हैं। अम्लवर्षा पत्थर एवं धातुओं से बनी संरचनाओं, भवनों, आदि को नष्ट करती है। हमारे देश में ताजमहल जैसी ऐतिहासिक इमारतें अम्लवर्षा से दुष्प्रभावित हो रही हैं।
क्रियाकलाप-1
आप अपने नजदीकी क्षेत्रों के जल से विभिन्न नमूने एकत्र करके उनकी pH ज्ञात करें। परिणामों की चर्चा अपनी कक्षा में करें। आइए, इस बात पर चर्चा करें कि अम्लवर्षा को कम कैसे किया जाए।
वायुमंडल में सल्फर डाइअॉक्साइड (SO2) तथा नाइट्रोजन डाइअॉक्साइड (NO2) के उत्सर्जन को कम करके अम्लवर्षा को कम किया जा सकता है। हमें यातायात के व्यक्तिगत साधनों का कम प्रयोग करना चाहिए तथा शक्ति-संयंत्रों एवं उद्योगों में कम सल्फर मात्रा वाला जीवाश्म ईंधन काम में लेना चाहिए। हमें कोयले के स्थान पर प्राकृतिक गैस का प्रयोग या कम सल्फर से युक्त कोयले को ईंधन के रूप में काम में लाना चाहिए। कार में उत्प्रेरकीय परिवर्तक उपयोग में लेने चाहिए, ताकि वह वायुमंडल में उत्सर्जित धूम्र के प्रभाव को न्यूनतम कर सके। उत्प्रेरकीय परिवर्तन का प्रमुख अवयव सिरेमिक निर्मित मधुकोश होता है, जिस पर दुर्लभ धातुओं (जैसे– Pd, Pt तथा Rh) की परत चढ़ी होती है। निर्गमित गैस, जिसमें बिना जला ईंधन CO तथा NOx होते हैं, को जब 573K पर उत्प्रेरकीय परिवर्तक में से गुजारा जाता है, तब यह इन्हें CO2 तथा N2 में परिवर्तित कर देता है। हम मृदा में चूर्णीय चूना- पत्थर मिलाकर मृदा की अम्लीयता को कम कर सकते हैं। अधिकतर व्यक्ति अम्लवर्षा तथा इसके हानिकारक प्रभावोें के बारे में नहीं जानते हैं। हम उन्हें सूचनाएँ देकर जागरूक कर सकते हैं तथा प्रकृति को बचा सकते हैैं।
ताजमहल एवं अम्लवर्षा
आगरा शहर में स्थित ताजमहल के चारों ओर की वायु में सल्फर तथा नाइट्रोजन अॉक्साइड की उच्च सांद्रता उपस्थित है। यह इस क्षेत्र के चारों ओर अधिक मात्रा में शक्ति संयंत्र एवं उद्योगों के कारण है। घरेलू कार्यों में ईंधन के रूप में न्यून गुणवत्ता वाला कोयला, केरोसिन तथा लकड़ी का उपयोग करने पर यह समस्या बढ़ती है, जिसके फलस्वरूप अम्लवर्षा ताजमहल के संगमरमर (CaCO3) से क्रिया करती है
(CaCO3 + H2SO4 → CaSO4 + H2O + CO2) तथा संपूर्ण विश्व को आकर्षित करने वाले इस अद्भुत स्मारक को हानि पहुँचाती है। अम्लवर्षा के कारण यह स्मारक धीरे-धीरे क्षत हो रहा है तथा अपना प्राकृतिक रंग एवं आभा खोता जा रहा है। इस स्मारक को नष्ट होने से बचाने के लिए भारत सरकार ने सन् 1995 में एक कार्य-योजना प्रारंभ करने की घोषणा की। मथुरा तेलशोधन संयंत्र ने विषैली गैसों के उत्सर्जन को नियंत्रित करने के लिए पूर्व में ही उपयुक्त कदम उठा लिए हैं।
इस योजना के अंतर्गत ‘ताज ट्रैपीज़ियम’ की वायु को स्वच्छ करना है। इस क्षेत्र में आगरा, फीरोज़ाबाद, मथुरा तथा भरतपुर नगर सम्मिलित हैं। इसके अनुसार, ट्रैपीज़ियम स्थित 2000 से भी अधिक उद्योग ईंधन के रूप में कोयला अथवा तेल के स्थान पर प्राकृतिक गैस अथवा एल.पी.जी. का उपयोग करेेंगे। इसके लिए एक नयी प्राकृतिक गैस पाइप लाइन बिछाई जा रही है, जिसकी सहायता से इस क्षेत्र में प्रतिदिन 5 लाख घनमीटर प्राकृतिक गैस लाई जाएगी। शहरों में रहनेवाले व्यक्तियों को इस बात के लिए प्रोत्साहित किया जाएगा कि वे दैनिक जीवन में कोयले, केरोसीन अथवा लकड़ी के स्थान पर एल.पी.जी. का ही उपयोग करें। इसके अतिरिक्त ताज के आसपास के राष्ट्रीय राजमार्गों पर चलने वाले यातायात के साधनों में कम सल्फर से युक्त डीजल का उपयोग करने के लिए प्रेरित किया जाएगा।
2. कणिकीय प्रदूषक
कणिकीय पदार्थ वायु में निलंबित सूक्ष्म ठोस कण अथवा द्रवीय बूँद होते हैं। यह मोटरवाहनों के उत्सर्जन, अग्नि के धूम्र, धूलकण तथा उद्योगों की राख होते हैं। वायुमंडल में कणिकाएँ जीवित तथा अजीवित-दोनों प्रकार की हो सकती हैं। जीवित कणिकाओं में जीवाणु, कवक, फफूंद, शैवाल आदि सम्मिलित हैं। हवा में पाए जाने वाले कुछ कवक मनुष्य में एलर्जी उत्पन्न करते हैं। ये पौधों के रोग भी उत्पन्न कर सकते हैं।
कणिकाओं को उनकी प्रकृति एवं आकार के आधार पर इस प्रकार वर्गीकृत किया जा सकता है-
(क) धूम कणिकाओं में ठोस एवं ठोस-द्रव कणों के मिश्रण होते हैं, जो कार्बनिक द्रव्य के दहन के दौरान उत्पन्न होते हैं। जैसे–सिगरेट का धुआँ, जीवाश्म ईंधन के दहन से प्राप्त ध्रूम, गंदगी का ढेर, सूखी पत्तियाँ, तेल-धूम्र आदि।
(ख)धूल में बारीक छोटे कण (व्यास 1-4µm से ऊपर) होते हैं, जो ठोस पदार्थों के पीसने, कुचलने एवं आरोपण से बनते हैं। ब्लास्ट से प्राप्त बालू, लकड़ी के कार्य से प्राप्त लकड़ी का बुरादा, कोयले का बुरादा, कारखानों से उड़ने वाली राख एवं सीमेन्ट, धुएँ के गुबार आदि इस प्रकार के उत्सर्जन के कुछ प्रारूपिक उदाहरण हैं।
(ग) फैले हुए द्रव-कणों एवं वाष्प के हवा में संघनन से कोहरा उत्पन्न होता है। उदाहरणार्थ–सल्फ्यूरिक अम्ल का कोहरा तथा शाकनाशी एवं कीटनाशी, जो अपने लक्ष्य से भटककर हवा से गमन करते हैं एवं कोहरा बनाते हैं।
(घ) धूम्र साधारणतया वाष्पों के ऊर्ध्वपातन, आसवन, क्वथन एवं अन्य रासायनिक अभिक्रियाओं के दौरान संघनन के कारण बनते हैं। प्रायः कार्बनिक विलायक-धातुएँ एवं धात्विक अॉक्साइड धूम्र-कणों का निर्माण करते हैं।
कणिक प्रदूषकों का प्रभाव मुख्यतया उनके कणों के आकार पर निर्भर करता है। हवा में ले जाए जानेवाले कण, जैसे-धूल, धूम, कोहरा आदि मानवीय स्वास्थ्य के लिए हानि- कारक हैं। 5 माइक्रोन से बड़े कणिक प्रदूषक नासिकाद्वार में जमा हो जाते हैं, जबकि लगभग 1-0 माइक्रोन के कण फेफड़ों में आसानी से प्रवेश कर जाते हैं।
वाहनों द्वारा उत्सर्जित लेड एक मुख्य वायु-प्रदूषक है। लेडयुक्त पेट्रोल भारतीय शहरों में वायुधारित लेड-उत्सर्जन का मुख्य ड्डोत है। अधिकतर शहरों में लेडविहीन (सीसारहित) पेट्रोल का उपयोग करके इस समस्या पर काबू पाया जा सकता है। लाल रक्त कोशिकाओं के विकसित एवं परिपक्व होने में लेड बाधा उत्पन्न करता है।
धूम-कोहरा (Smog)
‘धूम-कोहरा’ शब्द ‘धूम’ एवं ‘कोहरे’ से मिलकर बना है। विश्व के अनेक शहरों में प्रदूषण इसका आम उदाहरण है। धूम कोहरे दो प्रकार के होते हैं
(क)सामान्य धूम कोहरा (जो ठंडी नम जलवायु में होता है) धूम, कोहरे एवं सल्फर डाइऑक्साइड का मिश्रण है। रासायनिक रूप से यह एक अपचायक मिश्रण है। अतः इसे ‘अपचायक धूम-कोहरा’ भी कहते हैं।
(ख)प्रकाश रासायनिक धूम कोहरा जो उष्ण, शुष्क एवं साफ धूपमयी जलवायु में होता है, स्वचालित वाहनों तथा कारखानों से निकलने वाले नाइट्रोजन के ऑक्साइडों तथा हाइड्रोकार्बनों पर सूर्यप्रकाश की क्रिया के कारण उत्पन्न होता है। प्रकाश रासायनिक धूम कोहरे की रासायनिक प्रकृति ऑक्सीकारक है। चूँकि इसमें ऑक्सीकारक अभिकर्मकों की सांद्रता उच्च रहती है, अतः इसे ‘ऑक्सीकारक धूम कोहरा’ कहते हैं।
प्रकाश रासायनिक धूम कोहरे का निर्माण (Formation Of Photochemical Smog)
जब जीवाश्म ईंधनों का दहन होता है, तब पृथ्वी के वातावरण में कई प्रदूषक उत्सर्जित होते हैं। इनमें से में दो प्रदूषक हाइड्रोकार्बन (अदहित ईंधन) एवं नाइट्रिक ऑक्साइड (NO) है। जब इन प्रदूषकों का स्तर पर्याप्त ऊँचा हो जाता है, तब सूर्यप्रकाश से इनकी अन्योन्य क्रिया के कारण शृंखला अभिक्रिया होती हैं, जिसमें छव् नाइट्रोजन डाइऑक्साइड (NO2) में परिवर्तित हो जाती है। यह NO2 सूर्यप्रकाश से ऊर्जा ग्रहण कर पुनः नाइट्रिक ऑक्साइड एवं मुक्त ऑक्सीजन में विघटित हो जाती है (चित्र 14-2)।
NO2 (g) 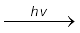 NO (g) + O (g) (i)
NO (g) + O (g) (i)
ऑक्सीजन परमाणु अत्यधिक क्रियाशील होने के कारण व O2 के साथ संयुक्त होकर ओजोन में परिवर्तित हो सकता है-
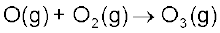 (ii)
(ii)
उपर्युक्त अभिक्रिया में निर्मित O3 शीघ्रतापूर्वक अभिक्रिया (1) में विरचित NO(g) के साथ अभिक्रिया कर पुनः NO2 बनाती है। NO2 एक भूरी गैस है, जिसका उच्च स्तर धुंध का कारण हो सकता है।
NO (g) + O3 (g) → NO2 (g) + O2 (g) (iii)
ओजोन एक जहरीली गैस है। NO2 एवं O3 दोनों ही प्रबल ऑक्सीकारक हैं। इस कारण प्रदूषित वायु में उपस्थित अदहित हाइड्रोकार्बनों के साथ अभिक्रिया करके कई रसायनों, जैसे-फार्मेल्डिहाइड, एक्रोलीन एवं परॉक्सीऐसीटिल नाइट्रेट (PAN) का निर्माण करते हैं।
प्रकाश रासायनिक धूम-कोहरे के प्रभाव
प्रकाश रासायनिक धूम्र कोहरे के सामान्य घटक ओजोन, नाइट्रिक अॉक्साइड, एक्रोलीन, फार्मेल्डिहाइड एवं परॉक्सीएेसीटिल नाइट्रेट (PAN) हैं। प्रकाश रासायनिक धूम-कोहरे के कारण भी गंभीर स्वास्थ्य-समस्याएँ होती हैं। ओजोन एवं नाइट्रिक ऑक्साइड नाक एवं गले में जलन पैदा करते हैं। इनकी उच्च सांद्रता से सरदर्द, छाती में दर्द, गले का शुष्क होना, खाँसी एवं श्वास अवरोध हो सकता है। प्रकाश रासायनिक धूम-कोहरा रबर में दरार उत्पन्न करता है एवं पौधों पर हानिकारक प्रभाव डालता है। यह धातुओं, पत्थरों, भवन-निर्माण के पदार्थों एवं रंगी हुई सतहों (Painted Surfaces) का क्षय भी करता है।
प्रकाश रासायनिक धूम-कोहरे का नियंत्रण कैसे किया जा सकता है?
प्रकाश रासायनिक धूम-कोहरे को नियंत्रित या कम करने के लिए कई तकनीकों का उपयोग किया जाता है। यदि हम प्रकाश रासायनिक धूम-कोहरे के प्राथमिक पूर्वगामी, जैसे–NO2एवं हाइड्रोकार्बन को नियंत्रित कर लें, तो द्वितीयक पूर्वगामी जैसे-ओजोन एवं च्।छ तथा प्रकाश रासायनिक धूम-कोहरा स्वतः ही कम हो जाएगा। सामान्यतया स्वचालित वाहनों में उत्प्रेरित परिवर्तक उपयोग में लाए जाते हैं, जो वायुमंडल में नाइट्रोजन ऑक्साइड एवं हाइड्रोकार्बन के उत्सर्जन को रोकते हैं।

चित्र 14.2 प्रकाश रासायनिक धूम-कोहरा वहाँ घटित होता है, जहाँ यातायात-प्रदूषकों परसूर्य का प्रकाश क्रिया करता है।
कुछ पौधों (जैसे-पाईनस, जुनीपेरस, क्वेरकस, पायरस तथा विटिस), जो नाइट्रोजन ऑक्साइड का उपापचय कर सकते हैं, का रोपण इस संदर्भ में सहायक हो सकता है।
14.2.2 समतापमंडलीय प्रदूषण
ओजोन का विरचन एवं विघटन
ऊपरी समतापमंडल में ओजोन (O3) की प्रचुर मात्र होती है, जो सूर्य से आनेवाले हानिकारक पराबैगनी (UV) विकिरणों (λ-225 nm) से हमें बचाती है। ये विकिरण त्वचा-कैन्सर (मेलोनोमा) के कारण बनते हैं। अतः ओजोन-कवच को बचाए रखना महत्त्वपूर्ण है।
पराबैगनी विकिरणों की डाइऑक्सीजन (अणु) से प्रतिक्रिया का उत्पाद समतापमंडल में उपस्थित ओजोन है। पराबैगनी विकिरण आणविक ऑक्सीजन को मुक्त ऑक्सीजन (व्) परमाणुओं में विखंडित कर देते हैं। आण्विक ऑक्सीजन से संयुक्त होकर ये ऑक्सीजन परमाणु ओजोन बनाते हैं।
ओजोन ऊष्मागतिकीय रूप से अस्थायी होती है एवं आण्विक ऑक्सीजन में विघटित हो जाती है। इस प्रकार ओजोन के निर्माण एवं विघटन में एक गतिकीय साम्य स्थापित हो जाता है। अभी हाल ही के वर्षों में समतापमंडल में कुछ रसायनों की उपस्थिति के कारण ओजोन की इस सुरक्षा-परत में अवक्षय की सूचनाएँ हैं। ओजोन परत में अवक्षय का मुख्य कारण क्लोरो- फ्लोरोकार्बन यौगिकों (CFCs) का उत्सर्जन है। जिन्हें ‘फ्रियोन’ भी कहा जाता है। ये यौगिक अक्रिय, अज्वलनशील, विषहीन कार्बनिक अणु हैं। अतः इनका उपयोग रेफ्रिजरेटर, एयर कन्डीशनर आदि में तथा प्लास्टिक फोम के निर्माण एवं कंप्यूटर उद्योग में कंप्यूटर के पुर्जों की सफाई करने में होता है।
CFCs एक बार वायुमंडल में उत्सर्जित होने पर वायुमंडल की अन्य गैसों से मिश्रित होकर सीधे समतापमंडल में पहुँच जाते हैं। समतापमंडल में ये शक्तिशाली विकिरणों द्वारा विघटित होकर क्लोरीन मुक्त मूलक उत्सर्जित करते हैं।
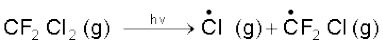 ...(i)
...(i)
क्लोरीन मुक्त मूलक तब समतापमंडलीय ओजोन से अभिक्रिया करके क्लोरीन मोनोअॉक्साइड मूलक तथा आण्विक अॉक्सीजन बनाते हैं।
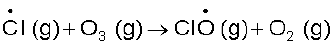 ...(ii)
...(ii)
क्लोरीन मोनोअॉक्साइड मूलक परमाण्विीय अॉक्सीजन के साथ अभिक्रिया करके अधिक क्लोरीन मूलक उत्पन्न करता है।
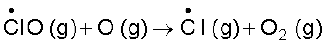 ...(iii)
...(iii)
क्लोरीन मूलक लगातार पुनर्याेजित होते रहते हैं एवं ओजोन को विखंडित करते हैं। इस प्रकार CFC समताप मंडल में क्लोरीन मूलकों को उत्पन्न करनेवाले एवं ओजोन-परत को हानि पहुँचाने वाले परिवहनीय कारक हैं।
ओजोन-छिद्र
सन् 1980 में वायुमंडलीय वैज्ञानिकों ने अंटार्कटिका पर कार्य करते हुए दक्षिणी ध्रुव के ऊपर ओजोन परत के क्षय, जिसे सामान्य रूप से ‘ओजोन-छिद्र’ कहा जाता है, के बारे में बताया।
यह पाया गया कि ओजोन छिद्र के लिए परिस्थितियों का एक विशेष समूह उत्तरदायी था। गरमी में नाइट्रोजन डाइअॉक्साइड परमाणुओं (अभिक्रिया iv) एवं क्लोरीन परमाणुओं (अभिक्रिया v) से अभिक्रिया करके क्लोरीन सिंक बनाते हैं, जो ओजोन-क्षय को काफी हद तक रोकता है।
जबकि सर्दी के मौसम में विशेष प्रकार के बादल, जिन्हें ‘ध्रुवीय समतापमंडलीय बादल’ कहा जाता है, अंटार्कटिका के ऊपर बनते हैं। ये बादल एक प्रकार की सतह प्रदान करते हैं, जिस पर बना हुआ क्लोरीन नाइट्रेट (अभिक्रिया iv) जलयोजित होकर हाइपोक्लोरस अम्ल बनाता है (अभिक्रिया vi)। अभिक्रिया में उत्पन्न हाइड्रोजन क्लोराइड से भी अभिक्रिया करके यह आण्विक क्लोरीन देता है।
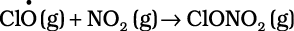 (iv)
(iv)
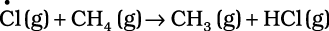 (v)
(v)
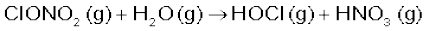 (vi)
(vi)
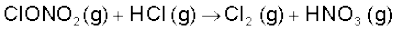 (vii)
(vii)
बसंत में अंटार्कटिका पर जब सूर्य का प्रकाश लौटता है, तब सूर्य की गरमी बादलों को विखंडित कर देती है एवं HOCl तथा Cl2 सूर्यप्रकाश से अपघटित हो जाते हैं (अभिक्रिया viii तथा ix)।
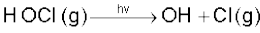 (viii)
(viii)
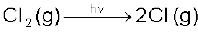 (ix)
(ix)
जैसा पूर्व में बताया गया है, उत्पन्न क्लोरीन मूलक, ओजोन-क्षय के लिए शृंखला अभिक्रिया प्रारंभ कर देते हैं।
ओजोन-परत के क्षय के प्रभाव
ओजोन परत के क्षय के साथ अधिकाधिक पराबैगनी विकिरण क्षोभमंडल में छनित होते हैं। पराबैगनी विकिरण से त्वचा का जीर्णन, मोतियाबिंद, सनबर्न, त्वचा-केन्सर, कई पादपप्लवकों की मृत्यु, मत्स्य उत्पादन की क्षति आदि होते हैं। यह भी देखा गया है कि पौधों के प्रोटीन पराबैगनी विकिरणों से आसानी से प्रभावित हो जाते हैं, जिससे कोशिकाओं का हानिकारक उत्परिवर्तन होता है। इससे पत्तियों के रंध्र से जल का वाष्पीकरण भी बढ़ जाता है, जिससे मिट्टी की नमी कम हो जाती है। बढ़े हुए पराबैगनी विकिरण रंगों एवं रेशों को भी हानि पहुँचाते हैं, जिससे रंग जल्दी हलके हो जाते हैं।
14.3 जल-प्रदूषण
जीवन के लिए जल अनिवार्य है। हम जल को साधारणतया शुद्ध मानते हैं, परंतु हमें जल की गुणवत्ता सुनिश्चित करनी चाहिए। जल का प्रदूषण मानवीय क्रियाकलापों से शुरू होता है। विभिन्न प्रक्रमों के माध्यम से प्रदूषण सतह या भौम जल तक आता है। प्रदूषण के सुज्ञात स्रोत या स्थानों को ‘बिंदु-स्रोत’ कहा जाता है। उदाहरण के लिए–नगरपालिका पाइप या औद्योगिक अपशिष्ट विसर्जन पाइप, जहाँ से प्रदूषक जल-स्रोत में प्रवेश करते हैं। प्रदूषण के अबिंदु स्रोत वे हैं, जहाँ पर प्रदूषण का स्रोत आसानी से पहचाना न जा सके। उदाहरणार्थ– कृषि-अपशिष्ट (खेतों, जानवरों एवं कृषि-भूमि से), अम्लवर्षा, तीव्र जल-निकासी (गलियों, उद्यानों, लॉन) आदि। सारणी 14.1 में जल के मुख्य प्रदूषण तथा उनके स्रोत दर्शाए गए हैं।
सारणी 14.1 मुख्य जल-प्रदूषक
| प्रदूषक | स्रोत |
| सूक्ष्म जीव कार्बनिक अपशिष्ट पादप पोषक विषाक्त भारी धातु तलछट पीड़कनाशी रेडियोधर्मी पदार्थ ऊष्मा | घरेलू सीवेज घरेलू सीवेज, पशु-अपशिष्ट, सड़े हुए मृत पशु तथा पौधे, खाद्य-संसाधन, कारखानों से विसर्जन रासायनिक उर्वरक उद्योग तथा रसायन कारखाने कृषि तथा विपट्टी खनन के कारण मृदा का अपरदन कीटों, कवक तथा खर-पतवार को नष्ट करने के लिए प्रयुक्त रसायन यूरेनियमयुक्त खनिजों का खनन औद्योगिक कारखानों द्वारा ठंडे पानी का उपयोग |
14.3.1 जल-प्रदूषण के कारण
(i) रोगजनक– सबसे ज्यादा गंभीर जल-प्रदूषक रोगों के कारकों को ‘रोगजनक’ कहा जाता है। रोगजनकों में जीवाणु एवं अन्य जीव हैं, जो घरेलू सीवेज एवं पशु-अपशिष्ट द्वारा जल में प्रवेश करते हैं। मानव-अपशिष्ट में एशरिकिआ कोली, स्ट्रेप्ट्रोकॉकस फेकेलिस आदि जीवाणु होते हैं, जो जठरांत्र बीमारियों के कारण होते हैं।
(ii) कार्बनिक अपशिष्ट–अन्य मुख्य जल-प्रदूषक कार्बनिक पदार्थ (जैसे–पत्तियाँ, घास, कूड़ा-कर्कट आदि) हैं। वे जल को प्रदूषित करते हैं। जल में पादप प्लवकों की अधिक बढ़ोतरी भी जल-प्रदूषण का एक कारण है।
बैक्टीरिया की बृहत् संख्या जल में कार्बनिक पदार्थों का अपघटन करती है। यह जल में विलेय अॉक्सीजन का उपभोग करती है। जल-विलयन में घुलित अॉक्सीजन सीमित होती है। ठंडे जल में घुलित अॉक्सीजन की सांद्रता 10 पीपीएम तक हो सकती है, जबकि वायु में यह करीब 2,00,000 पीपीएम है। यही कारण है कि जल में कार्बनिक पदार्थ के अपघटित होने की थोड़ी-सी मात्रा भी इसमें अॉक्सीजन का क्षय कर सकती है। जल में घुलित अॉक्सीजन जलीय जीवन के लिए बहुत महत्त्वपूर्ण है। यदि जल में घुलित अॉक्सीजन की सांद्रता 6 पीपीएम से नीचे हो जाए, तो मछलियों का विकास रुक जाता है। जल में अॉक्सीजन या तो वातावरण या कई जलीय पौधों द्वारा दिन में प्रकाश-संश्लेषण प्रक्रम से पहुँचती है। रात में प्रकाश-संश्लेषण रुक जाता है, परंतु पौधे श्वसन करते रहते हैं, जिससे जल में घुलित अॉक्सीजन कम हो जाती है। घुलित अॉक्सीजन सूक्ष्म जीवाणुओं द्वारा कार्बनिक यौगिकों के अॉक्सीकरण में भी उपयोग में ली जाती है।
यदि जल में बहुत अधिक कार्बनिक पदार्थ मिलाए जाएँ, तो उपलब्ध सारी अॉक्सीजन उपभोगित हो जाएगी। इसका परिणाम अॉक्सीजन-आश्रित जलीय जीवन की मृत्यु है। इस प्रकार अवायु जीवाणु, जिन्हें अॉक्सीजन की आवश्यकता नहीं होती है, कार्बनिक अपविष्ट का विखंडन आरंभ कर देते हैं एवं इससे दूषित गंध वाले रसायन उत्पन्न होते हैं, जो मानव-स्वास्थ्य के लिए हानिकारक हैं। वायु (अॉक्सीजन की आवश्यकता वाले) जीवाणु इन कार्बनिक अपविष्टों का विघटन करके जल को अॉक्सीजनरहित कर देते हैं।
अतः जल के एक नमूने के निश्चित आयतन में उपस्थित कार्बनिक पदार्थ को विखंडित करने के लिए जीवाणु द्वारा आवश्यक अॉक्सीजन को ‘जैवरासायनिक अॉक्सीजन माँग’ (BOD) कहा जाता है। अतः जल में BOD की मात्रा कार्बनिक पदार्थ को जैवीय रूप में विखंडित करने के लिए आवश्यक अॉक्सीजन की मात्रा होगी। स्वच्छ जल की BOD का मान 5 पीपीएम से कम होता है जबकि अत्यधिक प्रदूषित जल में यह 17 पीपीएम या इससे अधिक होता है।
(iii) रासायनिक प्रदूषक–हम जानते हैं कि जल एक अच्छा विलायक है। जल में विलेय अकार्बनिक रसायन, जिनमें भारी धातु (जैसे-केडमियम, मर्करी, निकेल आदि शामिल हैं) महत्त्वपूर्ण प्रदूषकों में आते हैं। ये सभी धातुएँ हमारे लिए हानिकारक हैं, क्योंकि हमारा शरीर इन्हें विसर्जित नहीं कर सकता है। समय के साथ इनकी मात्रा स्वीकार्य सीमा से ऊपर चली जाती है। तब ये प्रदूषक धातुओं, वृक्कों, केंद्रीय तंत्रिका-तंत्र, लीवर आदि को नुकसान पहुँचाते हैं। खदानों के सीवेज से प्राप्त अम्ल (जैसे–सल्फ्यूरिक अम्ल एवं विभिन्न स्रोतों से प्राप्त लवण, जिनमें ठंडे मौसम में हिम एवं बर्फ को पिघलाने वाले लवण– सोडियम एवं कैल्सियम क्लोराइड शामिल हैं) जल में विलेय प्रदूषक हैं।
प्रदूषित जल में पाए जाने वाले अन्य समूह कार्बनिक रसायन हैं। पेट्रोलियम उत्पाद (जैसे–समुद्रों में बड़े तेल-बहाव जल के कई स्रोतों को प्रदूषित करते हैं) दूसरे गंभीर प्रभाव वाले कार्बनिक यौगिकों में कीटनाशक हैं, जो स्प्रे द्वारा बहकर भूमि के नीचे आते हैं। विभिन्न प्रकार के औद्योगिक रसायन, जैसे–पॉलीक्लोरीनेटेड बाइफिनायल (PCBs), जो विलायक के रूप में प्रयुक्त होते हैं, अपमार्जक एवं उर्वरक भी जल-प्रदूषकों की श्रेणी में सम्मिलित हैं। PCBs संभावित कैन्सरजन्य हैं। आजकल उपलब्ध अधिकांश अपमार्जक जैव अपघटनीय हैं। फिर भी इनका उपयोग अन्य समस्याएँ उत्पन्न करता है। अपघटित करने वाले जीवाणु इन अपमार्जकों से भोजन प्राप्त करके तेजी से बढ़ते हैं। बढ़ोतरी करने में वे जल में उपस्थित समस्त अॉक्सीजन का उपयोग कर सकते हैं। अॉक्सीजन की कमी के कारण जलीय जीवन के अन्य रूप (जैसे–मछलियाँ एवं पौधे) मर सकते हैं। उर्वरकों में फॉस्फेट योगज के रूप में होते हैं। जल में फॉस्फेट का योग शैवाल की बढ़ोतरी को सहयोग करता है। शैवाल की यह प्रचुर बढ़ोतरी जलीय सतह को ढक लेती है तथा जल में अॉक्सीजन की सानुता बहुत कम हो जाती है फलतः अवायुविक परिस्थिति उत्पन्न होने से दुर्गंधा युक्त सडन पैदा होती है एवं जलीय जन्तुओं के मृत्यु का कारण बनती है। इस प्रकार यह पुष्पकुंजग्रस्त जल अन्य जीवों की वृद्धि को रोकता है। जल-निकायों में पौष्टिक अभिवृद्धि फलस्वरूप अॉक्सीजन की कमी के कारण सुपोषण (यूट्रोफिकेशन) कहते हैं।
14.3.2 जल के अंतरराष्ट्रीय मानक
पेय जल के अंतरराष्ट्रीय मानक, जिनका पालन होना चाहिए, नीचे दिए जा रहे हैं–
फ्लुओराइड–फ्लुओराइड आयन सांद्रता के लिए पेय जल का परीक्षण होना चाहिए। पेयजल में इसकी कमी मनुष्य के लिए हानिकारक है एवं कई बीमारियों (जैसे–दंतक्षय आदि) का कारण बनती है। अधिकांशतः पेयजल में विलयशीय फ्लुओराइड मिलाया जाता है, जिससे इसकी सांद्रता 1 ppm अथवा 1mg. dm–3 हो जाए। फ्लुओराइड आयन दाँतों के इनामेल सतह में हाइड्रॉक्सीएपेटाइट [3(Ca3(PO4)2 . Ca(OH)2] को फ्लुओएपेटाइट [3(Ca3(PO4)2 . CaF2] में परिवर्तित करके कड़ा कर देते हैं, यद्यपि फ्लुओराइड आयनों की 2 पीपीएम से अधिक की सांद्रता दाँतों के भूरे कर्बुरण (Mottling) उत्पन्न करती है। साथ ही फ्लुओराइड का आधिक्य (10 पीपीएम से अधिक) हड्डियों एवं दाँतों पर हानिकारक प्रभाव डालता है, जैसा राजस्थान के कुछ भागों में देखा गया है।
लेड–जब जल-परिवहन के लिए लेड पाइपों का उपयोग किया जाता है, तब जल लेड से दूषित हो जाता है। पीने के जल में लेड की निर्धारित ऊपरी सीमा लगभग 50 पीपीबी है। लेड किडनी, लीवर एवं पुनरुत्पादन-तंत्र को हानि पहुँचा सकता है।
सल्फेट–पेय जल में सल्फेट का आधिक्य (7500 पीपीएम) विरेचक का कारण हो सकता है। संतुलित स्तर पर रहने की दशा में सल्फेेट हानिरहित है।
नाइट्रेट–पीने के पानी में नाइट्रेट की अधिकतम सीमा 50 पीपीएम है। उसमें नाइट्रेट आधिक्य में होने पर मेथेमोग्लोबीनेमिया (ब्ल्यू बेबी सिन्ड्रोम) रोग हो सकता है।
अन्य धातुएँ– कुछ अन्य सामान्य धातुओं की अधिकतम सांद्रता सारणी 14.2 में दी गई है।
सारणी 14.2 पेय जल में निर्धारित सामान्य धातुओं की अधिकतम सांद्रता
| धातु | अधिकतम सांद्रता (ppm अथवा mgdm–3) |
| Fe Mn Al Cu Zn Cd | 0.2 0.05 0.2 3.0 5.0 0.005 |
क्रियाकलाप 2
आप स्थानीय जल-स्रोतों का निरीक्षण कर सकते हैं कि नदी, झील, हौद, तालाब आदि का पानी अप्रदूषित/ आंशिक प्रदूषित/ सामान्य प्रदूषित अथवा बुरी तरह प्रदूषित है। जल को देखकर या उसकी pH जाँचकर इसे देखा जा सकता है। निकट के शहरी या औद्योगिक स्थल, जहाँ से प्रदूषण उत्पत्र होता है, से उसके नाम का प्रलेख करें। इसकी सूचना सरकार द्वारा प्रदूषण-मापन के लिए गठित प्रदूषण नियंत्रण बोर्ड कार्यालय को दें तथा समुचित कार्यवाही सुनिश्चित करें। आप इसे मीडिया को भी बता सकते हैं। नदी, तालाब, जलधारा या जलाशय में घरेलू अथवा औद्योगिक अपविष्ट को सीधे नहीं डाले। बगीचों में रासायनिक उर्वरकों के स्थान पर कंपोस्ट का प्रयोग करें। डी.डी.टी., मैलाथियोन आदि कीटनाशी के प्रयोग से परहेज करें तथा यथासंभव नीम की सूखी पत्तियों का प्रयोग कीटनाशी के रूप में करें। अपनी घरेलू पानी टंकी में पौटेशियम परमैंग्नेट (KMnO4) की कुछ क्रिस्टल अथवा ब्लीचिंग पाउडर की थोड़ी मात्रा डालें।
14.4 मृदा-प्रदूषण
भारत एक कृषि-आधारित अर्थव्यवस्था वाला देश है, जहाँ कृषि, मत्स्य एवं पशुधन के विकास को प्राथमिकता दी जाती है। अकाल के समय के लिए अधिशेष उत्पादन का भंडारण सरकारी तथा गैर-सरकारी संस्थाओं द्वारा किया जाता है। भंडारण की अवधि में होने वाली खाद्य सामग्री की हानि पर विशेष ध्यान देना आवश्यक है। क्या आपने कभी कीट, कृतक, अपतमृण तथा फसलों की बीमारियों के द्वारा फसलों एवं खाद्य पदार्थों को होने वाली क्षति को देखा है? इन्हें हम कैसे बचा सकते हैं? फसलों के बचाव के लिए प्रयुक्त होने वाले कुछ कीटनाशी एवं पीडकनाशियों से आप परिचित हैं। ये कीटनाशी, पीडकनाशी तथा शाकनाशी मृदा-प्रदूषण के कारण हैं। अतः इनके विवेकपूर्ण प्रयोग की आवश्यकता है।
14.4.1 पीडकनाशी
द्वितीय विश्वयुद्ध से पूर्व प्राकृतिक रूप से पाए जाने वाले अनेक रसायनों, जैसे–निकोटीन (फसल के साथ खेत में तंबाकू के पौधे उगाकर) का प्रयोग अनेक फसलों के लिए पीडक-नियंत्रक पदार्थ के रूप में किया जाता था।
द्वितीय विश्वयुद्ध के समय मलेरिया तथा अन्य कीटजनित रोगों के नियंत्रण में डी.डी.टी. बहुत उपयोगी यौगिक पाया गया। इसीलिए युद्ध के पश्चात् डी.डी.टी. का उपयोग कृषि में कीट, सेडैंट, खर-पतवार तथा फसलों के अनेक रोगों के नियंत्रण के रूप में किया जाने लगा। हालाँकि प्रतिकूल प्रभावों के कारण इसका प्रयोग भारत में प्रतिबंधित हो गया है।
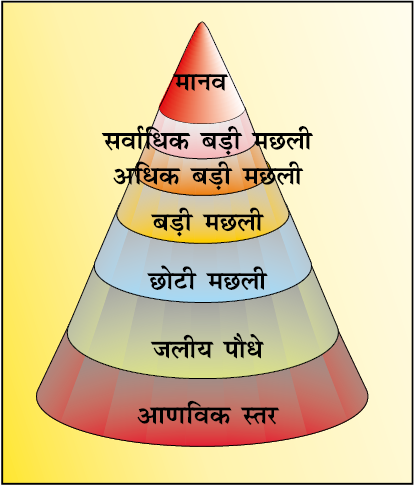
चित्र 14.3 प्रत्येक पोषी स्तर पर प्रदूषक दस गुना सांद्रित हो जाता है।
पीडकनाशी मूल रूप से संश्लेषित विषैले रसायन हैं, जो पारिस्थितिकी प्रतिघाती भी हैं। समान पीडकनाशकों के प्रयोग से कीटों में पीडकनाशकों के प्रति प्रतिरोध-क्षमता उत्पत्र हो जाती है, जो पीडकनाशी को प्रभावहीन बनाती है। इसीलिए डी.डी.टी. के प्रति प्रतिरोधकता में वृद्धि होने लगी, अन्य जीव-विष (जैसे–एेल्ड्रीन तथा डाइएेल्ड्रीन) पीडकनाशी उद्योग द्वारा बाजार में लाए गए। अधिकांश कार्बनिक जीव-विष जल में अविलेय तथा अजैवनिम्नीकरणीय होते हैं। ये उच्च प्रभाव वाले जीव-विष भोजन शृंखला द्वारा निम्नपोषी स्तर से उच्चपोषी स्तर तक स्थानांतरित होते हैं (चित्र 14.3) समय के साथ-साथ उच्च प्राणियों में जीव-विषों की सांद्रता इस स्तर तक बढ़ जाती है कि उपापचयी तथा शरीर क्रियात्मक अव्यवस्था का कारण बन जाती है।
उच्च स्थायित्व वाले क्लोरीनीकृत कार्बनिक जीव-विष के प्रत्युत्तर में निम्न स्थायित्व अथवा अधिक जैव निम्नीकरणीय उत्पादों, जैसे–आर्गेनो-फॉस्फेट्स तथा कार्बामेट्स को बाज़ार में लाया गया, परंतु ये रसायन गंभीर स्नायु जीव-विष हैं। अतः ये मानव के लिए अधिक हानिकारक हैं। परिणामस्वरूप एेसी घटनाएँ दर्ज हुई हैं, जिनमें खेतों में काम करने वाले मजदूरों की मृत्यु का कारण कुछ पीडकनाशी रहे हैं। कीट भी इन कीटनाशकों के प्रति प्रतिरोधी हो चुके हैं। पीडकनाशी उद्योग नए कीटनाशकों को विकसित करने में व्यस्त हैं, परंतु हमें सोचना पड़ेगा कि पीडकों के खतरे से निपटने का क्या यही एक साधन रह गया है?
इन दिनों पीडकनाशी उद्योग ने अपना ध्यान शाकनाशी, (जैसे–सोडियम क्लोरेट (NaClO3), सोडियम आर्सिनेट (Na3AsO3) आदि) की ओर मोड़ा है। गत शताब्दी के पूर्वार्द्ध में यांत्रिक से रासायनिक अपतृण नियंत्रण की ओर किए गए विस्थापन के कारण उद्योग को समृद्ध आर्थिक बाज़ार उपलब्ध हुआ है, परंतु हमें यह ध्यान रखना पड़ेगा कि यह भी पर्यावरण के अनुकूल नहीं है।
अधिकांश शाकनाशी स्तनधारियों के लिए विषैले होते हैं, परंतु ये कार्ब-क्लोराइड्स के समान स्थायी नहीं होते हैं। ये रसायन कुछ ही माह में अपघटित हो जाते हैं। कार्ब-क्लोराइड की भाँति ये भी पोषी स्तर पर सांद्रित हो जाते हैं। मानव में जन्मजात कमियों का कारण कुछ शाकनाशी हैं। यह पाया गया कि मक्का के खेत, जिनमें शाकनाशी का छिड़काव किया गया हो, कीटों के आक्रमण तथा पादप रोगों के प्रति उन खेतों से अधिक सुग्राही होते है, जिनकी निराई हाथों से की जाती है।
पीडकनाशी तथा शाकनाशी व्यापक रूप से फैले रासायनिक प्रदूषण के छोटे से भाग का प्रतिनिधित्व करते हैं। विभित्र वस्तुओं के उत्पादन के औद्योगिक एवं रासायनिक प्रक्रमों में निरंतर प्रयुक्त होने वाले अनेक यौगिक अंततः किसी न किसी रूप में वायुमंडल में मुक्त होते रहते हैं।
14.5 औद्योगिक अपशिष्ट
औद्योगिक ठोस अपशिष्ट (Solid waste) को जैव अपघटनी तथा जैव अनपघटनी ठोसों में वर्गीकृत किया जा सकता है। जैव अपघटनी अपशिष्ट सूत की मिलों, खाद्य-संसाधन इकाइयों, कागज की मिलों तथा वस्त्र उद्योगों द्वारा उत्पन्न होते हैं।
ऊष्मीय शक्ति संयंत्र, जो उड़न राख (Flyash) उत्पन्न करते हैं तथा लोहा एवं स्टील संयंत्र, जो वात्या भट्ठी धातुमल तथा स्टील प्रगलन धातुमल उत्पन्न करते हैं, के द्वारा जैव अनिम्नीकरण अपशिष्ट उत्पन्न होते हैं। एेलुमिनियम, जिंक तथा कॉपर के उत्पादन उद्योग, जो पंक तथा पछोडन (mud and tailing) उत्पन्न करते हैं। उर्वरक उद्योग जिप्सम का उत्पादन करता है। धातु, रसायन, दवा, फार्मेसी, रंजक, पीडकनाशी, रबर आदि से संबंधित उद्योग ज्वलनशील, मिश्रित विस्फोटक या उच्च क्रियाशील पदार्थ का उत्पादन करते हैं।
यदि जैव अनपघटनी औद्योगिक ठोस अपशिष्ट का सही तरीके से निस्तारण नहीं किया जाए, तो पर्यावरण के लिए गंभीर खतरा हो सकता है। अभिनव परिवर्तनों के फलस्वरूप अपशिष्ट पदार्थों के विभिन्न उपयोग खोज निकाले गए हैं। आजकल स्टील उद्योग से उत्पन्न फ्लाई एेश तथा धातुमल का उपयोग सीमेन्ट उद्योग में होने लगा है। भारी मात्रा में विषैले अपशिष्टों को सामान्यतः नियंत्रित भस्मीकरण द्वारा नष्ट किया जाता है, जबकि कम मात्रा में उत्पन्न अपविष्ट पदार्थों को खुले में जलाकर नष्ट कर दिया जाता है, परंतु ठोस अपशिष्टों का प्रबंधन यदि ढंग से न किया जाए, तो भी ये पर्यावरण को प्रभावित करते हैं।
14.6 पर्यावरण-प्रदूषण को नियंत्रित करने के उपाय
इस एकक में वायु-प्रदूषण, जल-प्रदूषण, मृदा-प्रदूषण एवं औद्योगिक प्रदूषण के अध्ययन के पश्चात् अब आप पर्यावरण प्रदूषण के नियंत्रण की आवश्यकता महसूस करने लगे होंगे। आप अपने समीप के पर्यावरण को कैसे बचा सकते हैं? आप अपने अड़ोस-पड़ोस में उपरोक्त प्रदूषणों के नियंत्रण के लिए क्या-क्या कदम उठा सकते हैं या क्रियाकलाप कर सकते हैं, इस बारे में विचार करें। यहाँ अपशिट प्रबंधन के उपायों के संबंध में एक विचार रखा जा रहा है।
14.6.1 अपशिष्ट का प्रबंधन
ठोस अपशिष्ट केवल वही नहीं है, जो आप अपने कचरादान में देखते हैं। बेकार घरेलू वस्तुओं के अतिरिक्त भी अनेक अपविष्ट हैं, जैसे–चिकित्सीय अपविष्ट, कृषि अपशिष्ट, औद्योगिक अपशिष्ट एवं खनिज अपशिष्ट। पर्यावरण के निम्नीकरण का एक मुख्य कारण अपशिष्टों का अनुपयुक्त विधि से किया गया निस्तारण है। इसीलिए अपशिष्ट का प्रबंधन परम आवश्यक है।
आपको भारत सरकार द्वारा प्रारम्भ किए गए स्वच्छ भारत अभियान अथवा क्लीन इंडिया मिशन के विषय में ज्ञात होगा।

स्वच्छ भारत अभियान का प्रतीक चिह्न
स्वच्छ भारत अभियान की बड़ी छत्रछाया में दो मिशन प्रारंभ किए गए हैं। यह हैं स्वच्छ भारत मिशन - शहरी (SBM-U) तथा स्वच्छ भारत मिशन - ग्रामीण (SBM-G)। स्वच्छ भारत मिशन - शहरी का मुख्य उद्देश्य भारत को खुले में शौच से मुक्त करना तथा ठोस कचरे का 100 प्रतिशत वैज्ञानिक प्रबन्धन प्राप्त करना है। स्वच्छ भारत मिशन - ग्रामीण का उद्देश्य सभी क्षेत्रों को राष्ट्रपिता महात्मा गाँधी की एक सौ पचासवीं वर्षगांठ, 2 अक्तूबर, 2019 तक सब प्रकार से स्वच्छ, स्वस्थ तथा खुले में शौच से मुक्त कर ग्रामीण जन जीवन की गुणवत्ता में सुधार लाना है।
यदि आपने स्वच्छ भारत मिशन में भाग लिया हो तो अपने व्यक्तिगत अनुभव लिखिए।
क्या आप अपशिष्ट के पुनर्चक्रण के बारे में जानते हैं?
• प्लास्टिक अपशिष्ट से प्राप्त ईंधन की उच्च अॉक्टेन दर होती है। इसमें लेड नहीं होता है तथा इसे ‘हरित ईंधन’ (Green fuel) कहते हैं।
• रसायन एवं वस्त्र उद्योग में किए गए आधुनिक विकास के कारण अब पुनः चक्रित प्लास्टिक से वस्त्र बनाए जाएँगे। ये जल्दी ही विश्व के वस्त्र-बाज़ार में उपलब्ध होंगे।
• हमारे देश में शहरों तथा कस्बों को बिजली की भीषण कटौती का सामना करना पड़ता है। चारों तरफ सड़ते हुए अपशिष्ट के ढेर भी हम देख सकते हैं। एक अच्छी खबर यह है कि हम इन दोनों समस्याओं से एक साथ छुटकारा पा सकते हैं। आजकल एक एेसी तकनीक विकसित की गई है, जिसमें कचरे से विद्युत् का उत्पादन होता है। एक प्रायोगिक संयंत्र लगाया गया है, जिसमें कचरे से लौह धातु को अलग करके प्लास्टिक, काँच, कागज आदि को पानी में मिलाया जाता है। बैक्टीरिया द्वारा इसका संवर्धन (Culture) कर मेथेन बनाते हैं, जिसे सामान्यतः ‘बायोगैस’ के नाम से जाना जाता है। बायोगैस का उपयोग बिजली के उत्पादन में होता है तथा शेष उत्पाद खाद के रूप में प्रयुक्त होता है।
एकत्रण तथा निस्तारण (Collection and disposal)
घरेलू अपशिष्ट को छोटे पात्रों में एकत्र करते हैं, जिसे सार्वजनिक कचरा-पात्रों में डाल दिया जाता है। इन सामुदायिक पात्रों में से इसे इकट्ठा करके निस्तारण-स्थल (dumping place) तक पहुँचाया जाता है। निस्तारण-स्थल पर कचरे को इकट्ठा कर इसे जैव अनिम्नीकरण अपशिष्टों तथा जैव निम्नीकरण अपशिष्टों में छाँटकर पृथक् कर लिया जाता है। जैव अनिम्नीकरण पदार्थों, जैसे–प्लास्टिक, काँच, धातु, छीलन आदि को पुनर्चक्रण (Recycling) के लिए भेज दिया जाता है। जैव निम्नीकरण अपशिष्ट को खुले मैदानों में मिट्टी में दबा दिया जाता है। जैव निम्नीकरण अपशिष्ट कंपोस्ट खाद (Compost) में परिवर्तित हो जाता है।
यदि अपशिष्ट को कचरा-पात्रों में इकट्ठा नहीं करें, तो वह नालियों में चला जाता है। इसमें से कुछ मवेशियों द्वारा खा लिया जाता है। जैव अनिम्नीकरण अपविष्ट (जैसे–पॉलिथीन की थैलियाँ, धातु-छीलन आदि) नालियों को रुद्ध कर देती हैं एवं असुविधा उत्पन्न करती हैं। पॉलिथीन की थैलियाँ यदि जन्तुओं द्वारा निगल ली जाएँ, तो उनकी मृत्यु का कारण भी बन सकती हैं। इसीलिए सामान्य व्यवहार में सभी घरेलू अपविष्ट सही तरीके से एकत्र करके इनका निस्तारण करना चाहिए। घटिया प्रबंधन से स्वास्थ्य-संबंधी अनेक समस्याएँ उत्पन्न होती हैं, जिससे भूमि के जल के प्रदूषण के कारण महामारियाँ फैलती हैं। यह विशेषतः उन लोगों के लिए अधिक हानिकारक है, जो इस अपशिष्ट के सीधे संपर्क में आते हैं, जैसे–पुराना सामान तथा कचरा इकट्ठा करने वाले और वे कर्मचारी, जो अपशिष्ट के निस्तार के काम में लगे रहते हैं, क्योंकि ये वे व्यक्ति हैं, जो अपशिष्ट को दस्ताने या जलरोधी जूतों को पहने बिना स्पर्श करते हैं और गैस-मास्क का भी उपयोग नहीं करते हैं। आप उनके लिए क्या कर सकते हैं?
14.7 हरित रसायन (ग्रीन केमिस्ट्री)
14.7.1 परिचय
यह सर्वविदित तथ्य है कि हमारे देश में 20वीं सदी के अंत तक उर्वरकों एवं कीटनाशकों के उपयोग तथा कृषि के उन्नत तरीकों का प्रयोग करके अच्छी किस्म के बीजों, सिंचाई आदि से खाद्यान्नों के क्षेत्र में आत्मनिर्भरता प्राप्त कर ली है, परंतु मृदा के अधिक शोषण एवं उर्वरकों तथा कीटनाशकों के अंधाधुंध उपयोग से मृदा, जल एवं वायु की गुणवत्ता घटी है।
येज चाउविन इन्स्टिच्यूट फ्रैंक्स, डू पेट्रोले, रूइनल-मेलमेसन, फ्रान्स, रॉबर्ट एच. ग्रुब्स, कैलिफोर्निया इन्स्टिच्यूट अॉफ टेक्नोलॉजी (कैलटेक), पासाडेना, सी.ए, यू.एस.ए. तथा रिचर्ड आर. श्रोक मासाच्युएट्स इन्स्टिच्यूट अॉफ टेक्नोलॉजी (एम.आई.टी.) कैंब्रिज,यू.एस.ए. ने नए रसायनों के निर्माण, जिनमें हानिकारक अपविष्ट कम होते हैं, पर कार्य करने के लिए सन् 2005 का नोबेल पुरस्कार पाया। तीनों ने कार्बनिक संश्लेषण की स्थानांतरण (मेटाथेसिस) विधि के लिए पुरस्कार पाया। इसमें अणु के अंदर परमाणु समूह पुनर्व्यवस्थित होते रहते हैं। रॉयल स्वीडिश अकादमी ने इसकी तुलना एेसे नृत्य से की है, जिसमें युगल अपना जोड़ीदार बदलते हैं। मेटाथेसिस का जबरदस्त वाणिज्यिक उपयोग औषधि, जैव तकनीकी एवं खाद्य उद्योग में है। इसका उपयोग पर्यावरणीय मैत्रीपूर्ण बहुलकों के क्रांतिकारी विकास में भी होता है।
यह हरित रसायन में एक बड़े कदम का प्रतिनिधित्व है। कुशल उत्पादन द्वारा हानिकारक अपविष्टों को कम किया जाता है। मेटाथेसिस इस बात का उदाहरण है कि मूल विज्ञान का उपयोग मनुष्य, समाज एवं पर्यावरण के लाभ के लिए कैसे प्रयुक्त किया गया है।
इस समस्या का समाधान विकास के प्रारंभ हो चुके प्रक्रम को रोकना नहीं, बल्कि उन तरीकों को खोजना है, जो वातावरण के बिगड़ने को रोक सकें। रसायन विज्ञान तथा अन्य विज्ञानों के उन सिद्धांतों का ज्ञान, जिससे पर्यावरण के दुष्प्रभावों को कम किया जा सके, ‘हरित रसायन’ कहलाता है। हरित रसायन उत्पादन का वह प्रक्रम है, जो पर्यावरण में न्यूनतम प्रदूषण या खराबी लाए। एक प्रक्रम में उत्पन्न होने वाले सह उत्पादों को यदि लाभदायक तरीके से उपयोग नहीं किया जाए तो वे पर्यावरण-प्रदूषण में सहायक होते हैं। एेसे प्रक्रम न सिर्फ पर्यावरणीय दृष्टि से हानिकारक हैं, बल्कि महँगे भी हैं। उत्पाद अपव्यय एवं इसका विसर्जन दोनों ही वित्तीय रूप से खराब हैं। विकास-कार्यों के साथ-साथ वर्तमान ज्ञान का रासायनिक हानि को कम करने के लिए उपयोग में लाना ही हरित रसायन का आधार है। क्या आपने हरित रसायन का विचार ग्रहण किया है? यह भली-भाँति ज्ञात है कि कार्बनिक विलायक, जैसे–बेंजीन, टॉलूइन, कार्बन टेट्राक्लोराइड आदि अत्यधिक विषैले हैं। इनका प्रयोग करते समय सतर्क रहना चाहिए।
जैसा आप जानते हैं, एक रासायनिक अभिक्रिया की सीमा, ताप, दाब, उत्प्रेरक के उपयोग आदि भौतिक मापदंड पर निर्भर करती हैं। यदि एक रासायनिक अभिक्रिया में अभिकारक एक पर्यावरणीय मैत्रीपूर्ण माध्यम में पूर्णतः पर्यावरणीय मैत्रीपूर्ण उत्पादों में बदल जाए, तो पर्यावरण में कोई रासायनिक प्रदूषक नहीं होगा।
संश्लेषण के दौरान प्रारंभिक पदार्थ का चयन करते समय यह सावधानी रखनी चाहिए, ताकि जब भी वह अंतिम उत्पाद में परिवर्तित हो, तो अपविष्ट उत्पन्न ही न हो। यह संश्लेषण के दौरान अनकूल परिस्थितियों को अर्जित करके किया जाता है। जल की उच्च विशिष्ट ऊष्मा तथा कम वाष्पशीलता के कारण इसे संश्लेषित अभिक्रियाओं में माध्यम के रूप में प्रयुक्त किया जाना वांछित है। जल सस्ता, अज्वलनशील तथा अकैंसरजन्य प्रभाव वाला माध्यम है।
14.7.2 दैनिक जीवन से हरित रसायन–
(i) कपड़ों की निर्जल धुलाई में
टेट्राक्लोरोएथीन [Cl2C = CCl2] का उपयोग प्रारंभ में निर्जल धुलाई के लिए विलायक के रूप में किया जाता था। यह यौगिक भू-जल को प्रदूषित कर देता है। यह एक संभावित कैंसरजन्य भी है। धुलाई की प्रक्रिया में इस यौगिक का द्रव कार्बन डाइअॉक्साइड एवं उपयुक्त अपमार्जक द्वारा प्रतिस्थापित किया जाता है। हैलोजेनीकृत विलायक का द्रवित CO2 से प्रतिस्थापन भू-जल के लिए कम हानिकारक है।
आजकल हाइड्रोजन परॉक्साइड का उपयोग लॉन्ड्री में कपड़ों के विरंजन के लिए लिया जाता है, जिससे परिणाम तो अच्छे निकलते ही हैं, जल का कम उपयोग भी होता है।
(ii) पेपर का विरंजन
पूर्व में पेपर के विरंजन के लिए क्लोरीन गैस उपयोग में आती थी। आजकल उत्प्रेरक की उपस्थिति में हाइड्रोजन परॉक्साइड, जो विरंजन क्रिया की दर को बढ़ाता है, उपयोग में लाया जाता है।
(iii) रसायनों का संश्लेषण
औद्योगिक स्तर पर एथीन का अॉक्सीकरण आयनिक उत्प्रेरकों एवं जलीय माध्यम की उपस्थिति में करवाया जाए, तो लगभग 90% एेथेनॉल प्राप्त होता है।
संक्षेप में, हरित रसायन एक कम लागत उपागम है, जो कम पदार्थ, ऊर्जा-उपभोग एवं अपविष्ट जनन से संबंधित है।
(iv) गंदले जल को स्वच्छ करने के हरित उपाय
म्युनिस्पालिटी एवं उद्योगों के अपशिष्ट जल को स्वच्छ करने के लिए इमली के बीजों का चूर्ण एक प्रभावी सामग्री पाई गई है। यह सस्ता होता है, विषैला नहीं होता और जैव निम्नीकृत हो सकता है। यह चूर्ण सामान्यतः कृषि अपशिष्ट की तरह फेंक दिया जाता है। आजकल एेसे जल को स्वच्छ करने के लिए फिटकरी का प्रयोग किया जाता है। यह पाया गया है कि फिटकरी विषैले आयनों की वृद्धि कर देती है तथा बीमारी का कारण बनती है।
इस बारे में सोचिए
मानव होने के नाते पर्यावरण को सुरक्षित रखने के लिए हमारी क्या ज़िम्मेदारी है?
किसी मानव द्वारा दी गई धारणाएँ मानव-जीवन तथा पर्यावरण-स्तर को उच्च बनाने में योगदान करती हैं। आपके बगीचे अथवा घर की किसी जगह में कंपोस्ट टिन का डिब्बा होना चाहिए तथा इसका प्रयोग पौधों के लिए खाद बनाने के कार्य में करना चाहिए, ताकि उर्वरकों का प्रयोग कम करना पड़े। हमें बाजार से फल, सब्जी तथा परचूनी का सामान एवं अन्य वस्तुएँ खरीदते समय कपड़ों के थैलों का उपयोग करके प्लास्टिक की थैलियों के उपयोग से बचना चाहिए। आप देखिए कि आपके क्षेत्र में पुराने समाचार-पत्रों, काँच, एेलεुमनियम तथा अन्य सभी वस्तुओं का पुनर्चक्रीकरण हो रहा है अथवा नहीं। पर्यावरण-सुरक्षा के लिए हमें एेसे विक्रेताओं को पहचान करने में थोड़ी परेशानी भी हो सकती है। हमें यह जानना चाहिए कि प्रत्येक समस्या का निवारण नहीं हो सकता है, किंतु हम अपना ध्यान उन पहलुओं पर केंद्रित कर सकते हैं, जिन्हें हम मुख्य रूप से महसूस कर सकें तथा उसके लिए कुछ कर सकें। जो कुछ भी हम कहते हैं, उस पर अमल भी करना चाहिए। हमें यह याद रखना चाहिए कि पर्यावरण संरक्षण सदैव हम से ही प्रारंभ होता है।
सारांश
पर्यावरणीय रसायन पर्यावरण में मुख्य भूमिका निभाता है। पर्यावरण में उपस्थित रसायन स्पीशीज़ कुछ प्राकृतिक हैं तथा अन्य मनुष्यों के कार्यकलापों से जनित पर्यावरण-प्रदूषण वातावरण में अनचाहे परिवर्तन का प्रभाव है, जो पौधों, जानवरों तथा मानव के लिए हानिकारक है। पदार्थ की सभी (तीनों) अवस्थाओं में प्रदूषक विद्यमान रहते हैं। हमने केवल उन्हीं प्रदूषकों का वर्णन किया है, जो मानव-क्रियाकलापों के फलस्वरूप उत्पन्न होते हैं और जिन्हें नियंत्रित किया जा सकता है। वायुमंडलीय प्रदूषण का अध्ययन सामान्यतया क्षोभमंडलीय एवं समतापमंडलीय प्रदूषण के रूप में किया जाता है। क्षोभमंडल वायुमंडल का निम्नतम स्तर (~10 km) है, जिसमें मानव के साथ अन्य जीव तथा वनस्पति भी सम्मिलित हैं, जबकि समतापमंडल क्षोभमंडल की ऊपरी सीमा से 40 किमी. ऊपर अर्थात् समुद्र-तल से 50 किलोमीटर की ऊँचाई तक स्थित है। ओजोन-परत समतापमंडल का एक प्रमुख घटक है। क्षोभमंडलीय प्रदूषण मूलतः सल्फर, नाइट्रोजन, कार्बन, हैलोजेन के अॉक्साइड तथा कणिकामय प्रदूषण के कारण होता है। क्षोभमंडल प्रदूषक पृथ्वी पर अम्लवर्षा के रूप में आते हैं। पृथ्वी पर पहुँचने वाले सौर-ऊर्जा का 75% भाग भू-पृष्ठ द्वारा अवशोषित कर लिया जाता है और शेष वातावारण में पुनः विकिरित कर दिया जाता है। उपरोक्त वर्णित गैसें ऊष्मा को ग्रहण करके भू-मंडलीय तापन के लिए उत्तरदायी हैं। ये गैसें पृथ्वी पर जीवन के लिए भी उत्तरदायी हैं, जो जीवनयापन के लिए पृथ्वी पर सौर-ऊर्जा की उपयोगी मात्रा को ग्रहण करती हैं। ग्रीनहाउस गैसों में अधिकता से पृथ्वी के वायुमंडल का तापमान बढ़ता है, जिससे ध्रुवीय बर्फ पिघलने के कारण समुद्र-तल में वृद्धि हो सकती है। परिणामतः समुदतटीय क्षेत्र जलमग्न हो सकते हैं। कई मानव-क्रियाकलाप रसायन उत्पन्न कर रहे हैं, जो समतापमंडल में ओजोन-परत के क्षय के लिए उत्तरदायी है, जो ओजोन-छिद्र का निर्माण करते हैं। ओजोन-छिद्र के द्वारा पराबैंगनी विकिरणें पृथ्वी के वायुमंडल में प्रवेश करती हैं, जो जीनों में उत्परिवर्तन का कारण हैं। जल हमारे जीवन के लिए उपयोगी है, लेकिन यही जल अगर रोगाणु, कार्बनिक अपविष्ट तथा विषैली भारी धातुएँ, पीडकनाशी आदि द्वारा प्रदूषित हो जाए तो यह विष में परिवर्तित हो जाता है। इसलिए अंतरराष्ट्रीय मानकों के अनुसार, हमें पेय जल के शुद्धता-स्तर को ध्यान में रखना चाहिए। औद्योगिक अपशिष्टों तथा पीडकनाशियों के अत्यधिक प्रयोग से भूमि तथा जल का प्रदूषण हुआ है। कृषि-क्षेत्र में रसायनों का युक्तिसंगत उपयोग विकास जारी रखने के लिए आवश्यक है। वातावरणीय प्रदूषण को नियंत्रित करने के लिए कई उपाय हैं, जैसे– (i) अपशिष्टों का प्रबंधन, अपशिष्टों में कमी करना, उनका अच्छी तरह सन्निक्षेपण तथा पदार्थ एवं ऊर्जा का पुनर्चक्रण करना (ii) दैनिक-जीवन में एेसी विधियों का उपयोग करना, जिससे वातावरणीय प्रदूषण कम हो। इसकी दूसरी विधि रसायन की नवीन शाखा है, जिसे हरित रसायन के नाम से जाना जाता है। इससे उपयुक्त ज्ञान एवं प्रयास से प्रदूषकों का उत्पादन यथासंभव कम कर दिया जाता है।
अभ्यास
14.1 पर्यावरणीय रसायन शास्त्र को परिभाषित कीजिए।
14.2 क्षोभमंडलीय प्रदूषण को लगभग 100 शब्दों में समझाइए।
14.3 कार्बन डाइअॉक्साइड की अपेक्षा कार्बन मोनोअॉक्साइड अधिक खतरनाक क्यों है? समझाइए।
14.4 ग्रीनहाउस-प्रभाव के लिए कौन सी गैसें उत्तरदायी हैं? सूचीबद्ध कीजिए।
14.5 अम्लवर्षा मूर्तियों तथा स्मारकों को कैसे दुष्प्रभावित करती है?
14.6 धूम कुहरा क्या है? सामान्य धूम कुहरा प्रकाश रासायनिक धूम कुहरे से कैसे भिन्न है?
14.7 प्रकाश रासायनिक धूम कुहरे के निर्माण के दौरान होने वाली अभिक्रिया लिखिए।
14.8 प्रकाश रासायनिक धूम कुहरे के दुष्परिणाम क्या हैं? इन्हें कैसे नियंत्रित किया जा सकता है?
14.9 क्षोभमंडल पर ओजोन-परत के क्षय में होने वाली अभिक्रिया कौन सी है?
14.10 ओजोन छिद्र से आप क्या समझते हैं? इसके परिणाम क्या हैं?
14.11 जल-प्रदूषण के मुख्य कारण क्या हैं? समझाइए।
14.12 क्या आपने अपने क्षेत्र में जल-प्रदूषण देखा है? इसे नियंत्रित करने के कौन से उपाय हैं?
14.13 आप अपने ‘जीव रसायनी अॉक्सीजन आवश्यकता’ (B.O.D) से क्या समझते हैं?
14.14 क्या आपने आस-पास के क्षेत्र में भूमि-प्रदूषण देखा है? आप भूमि-प्रदूषण को नियंत्रित करने के लिए क्या प्रयास करेंगे?
14.15 पीडकनाशी तथा शाकनाशी से आप क्या समझते है? उदाहरण सहित समझाइए।
14.16 हरित रसायन से आप क्या समझते हैं? यह वातावरणीय प्रदूषण को रोकने में किस प्रकार सहायक है?
14.17 क्या होता, जब भू-वायुमंडल में ग्रीनहाउस गैसें नहीं होतीं? विवेचना कीजिए।
14.18 एक झील में अचानक असंख्य मृत मछलियाँ तैरती हुई मिलीं। इसमें कोई विषाक्त पदार्थ नहीं था, परंतु बहुतायत में पादप्लवक पाए गए। मछलियों के मरने का कारण बताइए।
14.19 घरेलू अपविष्ट किस प्रकार खाद के रूप में काम आ सकते हैं?
14.20 आपने अपने कृषि-क्षेत्र अथवा उद्यान में कंपोस्ट खाद के लिए गड्ढे बना रखे हैं।
उत्तम कंपोस्ट बनाने के लिए इस प्रक्रिया की व्याख्या दुर्गंध, मक्खियों तथा अपविष्टों के चक्रीकरण के संदर्भ में कीजिए।