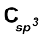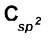Table of Contents
एकक
11
एेल्कोहॉल,फ़ीनॉल एवं ईथर
एेल्कोहॉल,फ़ीनॉल और ईथर क्रमशः अपमार्जक, पूतिरोधी एवं सुगंधि बनाने के मूल यौगिक हैं।
उद्देश्य
इस एकक के अध्ययन के पश्चात् आप -
• एेल्कोहॉलों,फ़ीनॉलों तथा ईथरों के नामकरण IUPAC नामपद्धति के अनुसार कर पाएंगे।
• एेल्कीनों, एेल्डिहाइडों, कीटोनों तथा कार्बोक्सिलिक अम्लों से एेल्कोहॉलों को बनाने की अभिक्रियाओं की विवेचना कर सकेंगे।
• हैलोएेरीनों, बेन्जीन सल्फोनिक अम्ल, डाइएेज़ोनियम लवणों तथा क्यूमीन सेफ़ीनॉलों को बनाने की अभिक्रियाओं की व्याख्या कर सकेंगे।
• एेल्कोहॉलों, एेल्किल हैलाइडों तथा सोडियम एेल्कॉक्साइडों / एेरिल अॉक्साइडों से ईथरों के विरचन की अभिक्रियाओं की व्याख्या कर
सकेंगे।
• एेल्कोहॉलों,फ़ीनॉलों और ईथरों के भौतिक गुणधर्मों एवं उनकी संरचनाओं को सहसंबंधित कर सकेंगे।
• प्रकार्यात्मक समूहों के आधार पर तीनों वर्गों के यौगिकों की रासायनिक अभिक्रियाओं की व्याख्या कर सकेंगे।
आपने पढ़ा है कि किसी हाइड्रोकार्बन के एक या उससे अधिक हाइड्रोजन परमाणुओं के दूसरे परमाणु या परमाणुओं के समूहों द्वारा प्रतिस्थापन से पूर्णतः नए यौगिकों का निर्माण होता है, जिनके गुणधर्म और अनुप्रयोग बिलकुल भिन्न होते हैं। जब एेलिफ़ैटिक और एेरोमैटिक हाइड्रोकार्बन का कोई हाइड्रोजन परमाणु हाइड्रॉक्सिल समूह द्वारा प्रतिस्थापित होता है तो क्रमशः एेल्कोहॉल तथा फ़ीनॉल बनते हैं। इन वर्गों के यौगिकों के, उद्योगों और हमारे दैनिक जीवन में अनेक अनुप्रयोग हैं। उदाहरणार्थ, क्या आपने कभी ध्यान दिया है कि लकड़ी केफ़र्नीचर की पॉलिश में प्रयुक्त होने वाली सामान्य स्प्रिट मुख्य रूप से हाइड्रॉक्सिल समूह युक्त यौगिक एथेनॉल है। खाद्य शर्करा, वस्त्रों में प्रयुक्त कपास, लिखने के लिए कागज़, सभी –OH समूह युक्त यौगिकों से निर्मित हैं। आपज़रा, कागज़ के बिना जीवन के बारे में कल्पना करें; जब कोई पुस्तक, पुस्तिका, समाचार पत्र, मुद्रा-नोट, चैक, प्रमाणपत्र नहीं होंगे। सुन्दर चित्रों तथा रुचिकर कहानियों वाली पत्रिकाएं हमारे जीवन से विलुप्त हो जाएंगीं। यह वास्तव में एक भिन्न संसार होगा।
एेल्कोहॉल में एक अथवा अधिक हाइड्रॉक्सिल (–OH) समूह, एेलिफ़ैटिक तंत्र (R–OH) के कार्बन परमाणु (परमाणुओं) से सीधे जुड़े होते हैं जबकिफ़ीनॉल में हाइड्रॉक्सिल (–OH) समूह एेरोमैटिक तंत्र (Ar–OH) के कार्बन परमाणु (परमाणुओं) से सीधे जुड़े होते हैं।
एेल्कॉक्सी अथवा एेरिलॉक्सी (R–O/ArO) समूह द्वारा हाइड्रोजन के प्रतिस्थापन से यौगिकों का एक दूसरा वर्ग प्राप्त होता है; जिन्हें ईथर कहते हैं। उदाहरणार्थ, CH3OCH3 (डाइमेथिल ईथर)। आप यह भी कल्पना कर सकते हैं कि ईथर वह यौगिक हैं जो किसी एेल्कोहॉल अथवाफ़ीनॉल के हाइड्रॉक्सिल समूह की हाइड्रोजन के, किसी एल्किल या एरिल समूह द्वारा विस्थापन से बनती हैं।
इस एकक में, हम तीन वर्गों के यौगिकों के बारे में पढ़ेंगे; यह हैं– एेल्कोहॉल,फ़ीनॉल एवं ईथर।
११.१ वर्गीकरण
11.1.1 एल्कोहॉल मोनो, डाइ, ट्राइ एवं पॉलीहाइड्रिक एल्कोहॉल
यौगिकों के वर्गीकरण से उनका अध्ययन क्रमबद्ध एवं सरल हो जाता है। इसलिए आइए, हम पहले यह सीखें कि एेल्कोहॉलों, फ़ीनॉलों एवं ईथरों को किस प्रकार वर्गीकृत किया जाता है?
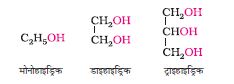
एेल्कोहॉलों औरफ़ीनॉलाें को उनके यौगिकों में उपस्थित एक (मोनो-), दो (डाइ-), तीन (ट्राइ-) अथवा अधिक हाइड्रॉक्सिल (–OH) समूहों की संख्या के अनुसार क्रमशः मोनो, डाइ, ट्राइ अथवा पॉलीहाइड्रिक यौगिकों में वर्गीकृत किया जाता है, जैसा कि निम्नलिखित संरचनाओं में दिखाया गया है–
मोनोहाइड्रिक एेल्कोहॉलों को हाइड्रॉक्सिल समूह से जुड़े कार्बन परमाणु की संकरण अवस्था के अनुसार पुनः वर्गीकृत किया जा सकता है।
(i) यौगिक जिनमें (![3258.png]() – OH) आबंध उपस्थित हो
– OH) आबंध उपस्थित हो
एेल्कोहॉलों के इस वर्ग में हाइड्रॉक्सिल (–OH) समूह एेल्किल समूह के sp3 संकरित कार्बन परमाणु से जुड़ा होता है। इन्हें पुनः निम्नलिखित प्रकार से वर्गीकृत किया जा सकता है–
प्राथमिक, द्वितीयक तथा तृतीयक एेल्कोहॉल—
इन तीन प्रकार के एेल्कोहॉलों में हाइड्रॅाक्सिल (–OH) समूह क्रमशः प्राथमिक, द्वितीयक तथा तृतीयक कार्बन परमाणु से जुड़ा होता है, जैसा कि नीचे दर्शाया गया है–

प्राथमिक (1°) द्वितीयक (2°) तृतीयक (3°)
एेलिलिक एेल्कोहॉल—
इस प्रकार के एेल्कोहॉल में –OH समूह, कार्बन-कार्बन द्विक्आबंध से अगले sp3 संकरित कार्बन परमाणु पर अर्थात् एेलिलिक कार्बन परमाणु से जुड़ा होता है।
उदाहरणार्थ–
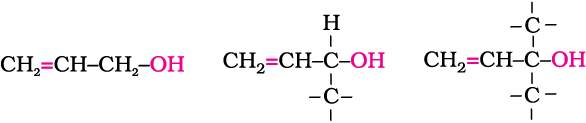
प्राथमिक द्वितीयक तृतीयक
बेन्ज़िलिक एेल्कोहॉल–
इस प्रकार के एेल्कोहॉल में –OH समूह एेरोमैटिक वलय से अगले sp3 संकरित कार्बन परमाणु पर जुड़ा होता है। उदाहरणार्थ–
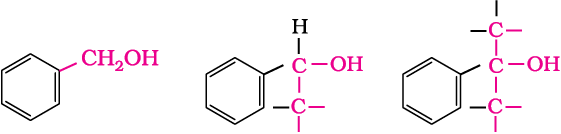
प्राथमिक द्वितीयक तृतीयक
एेलिलिक एवं बेंज़िलिक एेल्कोहॉल भी प्राथमिक, द्वितीयक अथवा तृतीयक हो सकती हैं।
(ii) यौगिक जिनमें (![3295.png]() – OH) आबंध उपस्थित हो
– OH) आबंध उपस्थित हो
11.1.2 .फीनॉल मोनो, डाइ एवं ट्राई हाइड्रिक.फीनॉल
.फीनोलों को भी हाइड्रॉक्सिल समूह की संख्या के अुनसार मोनो, डा ई एवं ट्राई हाइड्रिक .फीनोलों में वर्गीकृत किया जाता है।
फ़ीनॉल– 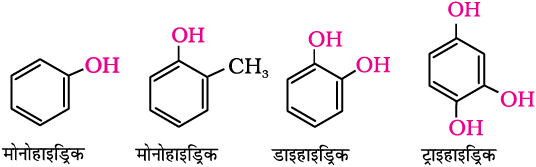
11.1.3 ईथर
ईथरों में यदि अॉक्सीजन परमाणु से जुड़े दोनों एेल्किल अथवा एेरिल समूह एक समान हों तो उन्हें सरल अथवा सममित ईथर और यदि ये दोनों समूह भिन्न-भिन्न हों तो इन्हें मिश्रित अथवा असममित ईथर में वर्गीकृत करते हैं।
C2H5OC2H5 एक सममित ईथर है जबकि C2H5OCH3 तथा C2H5OC6H5 असममित ईथर हैं।
पाठ्यनिहित प्रश्न
11.1 निम्नलिखित को प्राथमिक, द्वितीयक एवं तृतीयक एेल्कोहॉल में वर्गीकृत कीजिए–
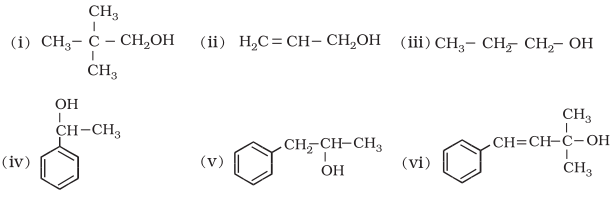
11.2 उपरोक्त उदाहरणों में से एेलिलिक एेल्कोहॉलों को पहचानिए।
११.२ नामपद्धति
(क) एेल्कोहॉल
एेल्कोहॉल के सामान्य नाम को व्युत्पन्न करने के लिए, हाइड्रॉक्सिल समूह से जुड़े एेल्किल समूह के सामान्य नाम के साथ एेल्कोहॉल शब्द जोड़ा जाता है। उदाहरणार्थ, CH3OH मेथिल एेल्कोहॉल है। आईयूपीएसी (IUPAC) पद्धति (एकक 12 कक्षा XI) के अनुसार एेल्कोहॉल का नाम व्युत्पन्न करने के लिए उस एेल्केन के अंग्रेज़ी में लिखे नाम के अंतिम 'e' को अनुलग्न अॉल (ol) से प्रतिस्थापित किया जाता है, जिससे उस एेल्कोहॉल की व्युत्पत्ति हुई है। प्रतिस्थापियों की स्थिति अंकों द्वारा इंगित की जाती है। इसके लिए सबसे लंबी कार्बन शृंखला (जनक शृंखला) का क्रमांकन उस सिरे से करते हैं जो हाइड्रॉक्सिल समूह के समीप हो। –OH समूह तथा अन्य प्रतिस्थापियों की स्थितियाँ उन कार्बन परमाणुओं के क्रमांक को प्रयुक्त कर दर्शाई जाती हैं जिससे वे जुड़े हों।
पॉलिहाइड्रिक एेल्कोहॉलों का नामकरण करने के लिए एेल्केन के अंग्रेज़ी के नाम का अंतिम e उसी प्रकार रखकर अंत में ‘अॉल’ जोड़ दिया जाता है। –OH समूहों की संख्या को ‘अॉल’ से पहले गुणात्मक पूर्वलग्न, डाइ, ट्राइ आदि लगाकर इंगित किया जाता है। –OH समूह की स्थिति को उपयुक्त स्थितिसूचक द्वारा इंगित करते हैं। उदाहरणार्थ–
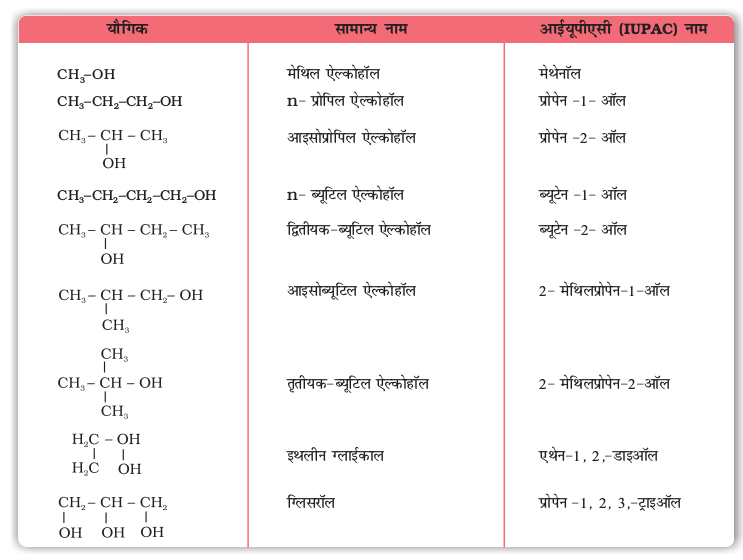
HO–CH2 –CH2–OH का नाम एथेन–1, 2-डाइअॉल है। सारणी 11.1 में कुछ एेल्कोहॉलों के सामान्य एवं आइयूपीएसी नाम दिए गए हैं।
सारणी 11.1– कुछ एेल्कोहॉलों के सामान्य तथा आईयूपीएसी नाम
चक्रीय एेल्कोहॉलों का नामकरण पूर्वलग्न साइक्लो लगाकर तथा –OH समूह को C–1 पर मानकर किया जाता है।

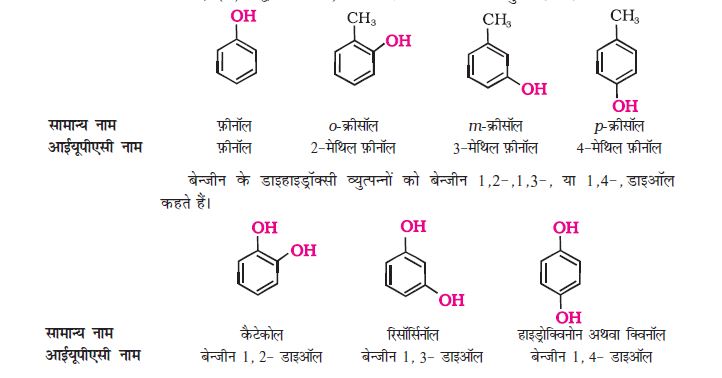
(ख)फ़ीनॉल
बेन्जीन का सबसे सरलतम हाइड्रॉक्सिल व्युत्पन्नफ़ीनॉल है। यह इसका सामान्य नाम तथा आईयूपीएसी द्वारा अनुमत नाम भी है। चूँकिफ़ीनॉल की संरचना में बेन्जीन वलय होती है अतः इसके प्रतिस्थापित यौगिकों में अॉर्थो (1,2 द्विप्रतिस्थापित), मेटा (1,3 द्विप्रतिस्थापित) तथा पैरा (1,4 द्विप्रतिस्थापित) भी प्रायः सामान्य नाम में प्रयुक्त होते हैं।
(ग) ईथर
उदाहरण के लिए CH3OC2H5 एथिल मेथिल ईथर है। यदि दोनों एेल्किल समूह समान हों तो एेल्किल समूह से पूर्वलग्न ‘डाइ’ लगाते हैं। उदाहरणार्थ–
CH3-CH2-O-CH2-CH3 डाइएथिल ईथर
आईयूपीएसी नामपद्धति में, ईथरों को हाइड्रोकार्बनों का व्युत्पन्न माना जाता है जिनके हाइड्रोजन परमाणु –OR समूह अथवा –OAr समूह द्वारा प्रतिस्थापित होते हैं, जहाँ R व Ar क्रमशः एेल्किल व एेरिल समूह हैं। इनमें बड़े एेल्किल (R) समूह को मूल हाइड्रोकार्बन चुना जाता है। कुछ ईथरों के नाम उदाहरण के रूप में सारणी 11.2 में दिए गए हैं।
सारणी 11.2– कुछ ईथरों के साधारण तथा आईयूपीएसी नाम
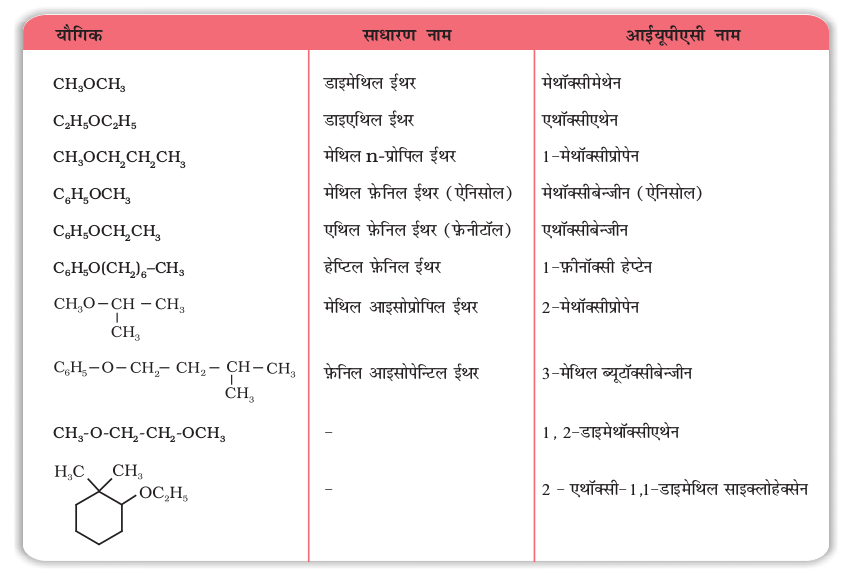
हल
कैटेकोल रिसॉर्सिनॉल हाइड्रोक्विनोन अथवा क्विनॉल
बेन्जीन 1, 2- डाइअॉल बेन्जीन 1, 3- डाइअॉल बेन्जीन 1, 4- डाइअॉल
पाठ्यनिहित प्रश्न
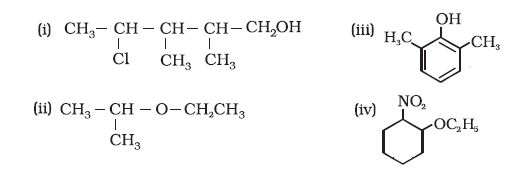
11.3 निम्नलिखित यौगिकों के आईयूपीएसी (IUPAC) नामपद्धति से नाम दीजिए–
(i) 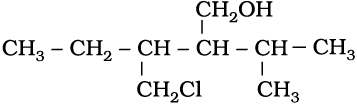
(ii) 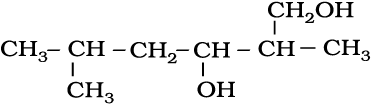
(iii) 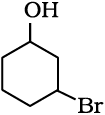
(iv) 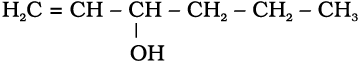
(v) 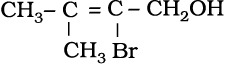
११.३ प्रकार्यात्मक समूहों की संरचनाएँ
एेल्कोहॉलों में –OH समूह की अॉक्सीजन कार्बन के साथ एक सिग्मा (σ) आबंध द्वारा जुड़ी होती है। जो कार्बन के sp3 संकरित कक्षक और अॉक्सीजन के sp3 संकरित कक्षक के अतिव्यापन द्वारा बनता है। चित्र 11.1 मेथेनॉल,फ़ीनॉल तथा मेथॉक्सीमेथेन के संरचनात्मक पहलुओं को प्रदर्शित करता है।
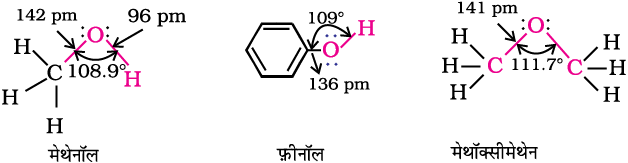
चित्र 11.1– मेथेनॉल,फ़ीनॉल तथा मेथॉक्सीमेथेन की संरचनाएँ
एेल्कोहॉलों में 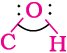 आबंध कोण चतुष्फलकीय कोण (109° 28′) से थोड़ा सा कम होता है। एेसा अॉक्सीजन के असहभाजित इलेक्ट्रॉन युगलों के मध्य प्रतिकर्षण के कारण होता है।फ़ीनॉलों में, –OH समूह एेरोमैटिक वलय के sp2 संकरित कार्बन के साथ जुड़ा होता है।फ़ीनॉलों के कार्बन-अॉक्सीजन आबंध की लंबाई (136 pm) मेथेनॉल में उपस्थित इस आबंध की लंबाई से थोड़ी कम होती है। इसका कारण है– (i) अॉक्सीजन के असहभाजित इलेक्ट्रॉन युगल का एेरोमैटिक वलय के साथ संयुग्मन होना; जिससे यह आबंध आंशिक द्विक्आबंध गुण प्राप्त करता है (खंड 11.4.4) एवं (ii) उस कार्बन की sp2 संकरित अवस्था, जिससे अॉक्सीजन जुड़ी है।
आबंध कोण चतुष्फलकीय कोण (109° 28′) से थोड़ा सा कम होता है। एेसा अॉक्सीजन के असहभाजित इलेक्ट्रॉन युगलों के मध्य प्रतिकर्षण के कारण होता है।फ़ीनॉलों में, –OH समूह एेरोमैटिक वलय के sp2 संकरित कार्बन के साथ जुड़ा होता है।फ़ीनॉलों के कार्बन-अॉक्सीजन आबंध की लंबाई (136 pm) मेथेनॉल में उपस्थित इस आबंध की लंबाई से थोड़ी कम होती है। इसका कारण है– (i) अॉक्सीजन के असहभाजित इलेक्ट्रॉन युगल का एेरोमैटिक वलय के साथ संयुग्मन होना; जिससे यह आबंध आंशिक द्विक्आबंध गुण प्राप्त करता है (खंड 11.4.4) एवं (ii) उस कार्बन की sp2 संकरित अवस्था, जिससे अॉक्सीजन जुड़ी है।
ईथरों में अॉक्सीजन पर उपस्थित चार इलेक्ट्रॉन युगल यानी कि दो आबंधी इलेक्ट्रॉन युगल और दो अनाबंधित इलेक्ट्रॉन युगल, लगभग चतुष्फलकीय रूप में व्यवस्थित होते हैं। दो स्थूल R समूहों के मध्य प्रतिकर्षक अन्योन्यक्रिया के कारण आबंध कोण चतुष्फलकीय कोण से थोड़ा अधिक होता है। ईथरों में C–O आबंध की लंबाई (141 pm); एेल्कोहॉलों के C–O आबंध की लंबाई के लगभग समान होती है।
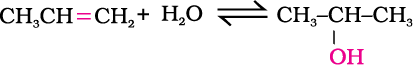
निम्नलिखित यौगिकों के आईयूपीएसी नाम लिखिए—
(i) 4-क्लोरो-2, 3-डाइमेथिलपेन्टेन-1-अॉल (iii) 2, 6-डाइमेथिलफ़ीनॉल
(ii) 2-एथॉक्सीप्रोपेन (iv) 1-एथॉक्सी-2-नाइट्रोसाइक्लोहेक्सेन
११.४ एेल्कोहॉलों और फ़ीनॉलों का विरचन
11.4.1 एेल्कोहॉलों का विरचन
एेल्कोहॉलों को निम्नलिखित विधियों द्वारा विरचित किया जाता है–
1. एेल्कीनो से
(i) अम्ल उत्प्रेरित जलयोजन द्वारा—
एेल्कीन तनु अम्ल की उत्प्रेरकों की तरह उपस्थिति में जल के साथ अभिक्रिया करके एेल्कोहॉल बनाती हैं। असममित एेल्कीनों में योगज अभिक्रिया मार्कोनीकॉफ नियम के अनुसार होती है (एकक 13, कक्षा XI)।
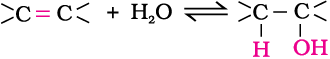
क्रियाविधि—
अभिक्रिया की क्रियाविधि में निम्नलिखित तीन चरण सम्मिलित होते हैं–
चरण 1–
H3O+ के इलेक्ट्रॉनरागी आक्रमण के द्वारा एेल्कीनों के प्रोटॉनन से कार्बोकैटायन बनते हैं।
H2O + H+ → H3O+
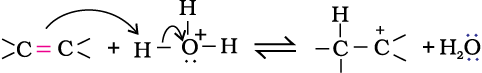
चरण 2–
कार्बोकैटायन पर जल का नाभिकरागी आक्रमण
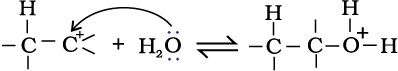
चरण 3–
विप्रोटोनन जिससे एेल्कोहॉल बनता है।
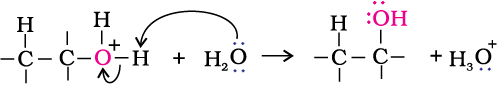
हाइड्रोबोरॉनन-आक्सीकरण का विवरण सर्वप्रथम एच.सी.ब्राउन द्वारा 1959 में दिया गया था। बोरॉनयुक्त कार्बनिक यौगिकों के अध्ययन के लिए ब्राउन ने 1979 में रसायन विज्ञान का नोबेल पुरस्कार, जी.विटिग के साथ संयुक्त रूप से प्राप्त किया।
(ii) हाइड्रोबोरॉनन-अॉक्सीकरण के द्वारा—
डाइबोरेन (BH3)2 एल्कीनों से अभिक्रिया करके एक योगज उत्पाद ट्राइएेल्किल बोरेन बनाता है जो जलीय सोडियम हाइड्राक्साइड की उपस्थिति में हाइड्रोजन परआक्साइड द्वारा अॉक्सीकृत होकर एेल्कोहॉल देता है।
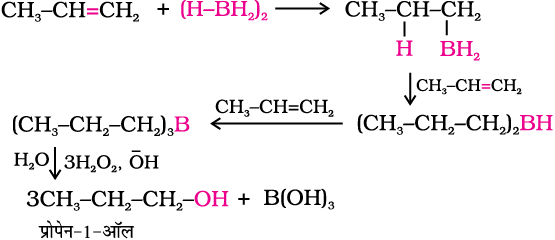
द्विक्आबंध पर बोरेन का योजन इस प्रकार होता है कि बोरॉन परमाणु, उस sp2 संकरित कार्बन परमाणु पर जुड़ता है जिस पर पहले से ही अधिक हाइड्रोजन परमाणु उपस्थित होते हैं। इस प्रकार प्राप्त एेल्कोहॉल, एेसी दिखती है जैसे कि यह एेल्कीनों से, मार्कोनीकॉफ के नियम के विपरीत जल योजन से बनी हो। इस अभिक्रिया में एेल्कोहॉलों की लब्धि उत्तम होती है।
2. कार्बोनिल यौगिकों से
तीर के निशान पर, अभिकर्मकों के नाम से पहले लिखी हुई संख्या इंगित करती है कि दूसरा अभिकर्मक तभी प्रयुक्त किया जाता है जब पहले अभिकर्मक के साथ अभिक्रिया पूर्णतः संपन्न हो जाती है।
(i) एेल्डिहाइड व कीटोन के अपचयन द्वारा—
एेल्डिहाइड एवं कीटोन उत्प्रेरक की उपस्थिति में हाइड्रोजन के योजन (उत्प्रेरकी हाइड्रोजनन) द्वारा संगत एेल्कोहॉलों में अपचित हो जाते हैं। सामान्यतः सूक्ष्म विभाजित धातु, जैसे–प्लैटिनम, पैलेडियम या निकैल उत्प्रेरक का कार्य करती हैं। ये एेल्डिहाइड और कीटोनों की सोडियम बोरोहाइड्राइड (NaBH4) अथवा लीथियम एेलुमिनियम हाइड्रॉइड (LiAlH4) के साथ अभिक्रिया द्वारा भी बनाई जा सकती हैं। एेल्डिहाइड प्राथमिक एेल्कोहॉल देते हैं, जबकि कीटोन द्वितीयक एेल्कोहॉल देते हैं।
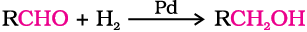
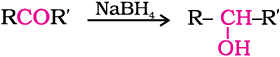
(ii) कार्बोक्सिलिक अम्लों तथा एस्टरों के अपयचन द्वारा—
कार्बोक्सिलिक अम्ल लीथियम एेलुमिनियम हाइड्राइड जैसे प्रबल अपचायक द्वारा अपचित हो जाते हैं और प्राथमिक एेल्कोहॉलों की उत्तम लब्धि देते हैं।
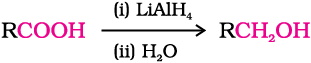
LiAlH4 एक महँगा अभिकर्मक है अतः इसका प्रयोग केवल विशेष रसायनों को बनाने के लिए किया जाता है। औद्योगिक स्तर पर कार्बोक्सिलिक अम्लों का एेल्कोहॉलों में अपचयन करने के लिए उन्हें एस्टर में परिवर्तित कर लिया जाता है (खंड 11.4.4) तत्पश्चात् उत्प्रेरक की उपस्थिति में एस्टर को हाइड्रोजन द्वारा अपचित कर लिया जाता है। (उत्प्रेरकी हाइड्रोजनन)
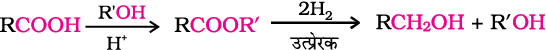
3. ग्रीन्यार अभिकर्मकों से
ग्रीन्यार अभिकर्मकों की एेल्डिहाइड और कीटोन के साथ अभिक्रिया कराने पर एेल्कोहॉल प्राप्त होती हैं (एकक 10, कक्षा XII)।
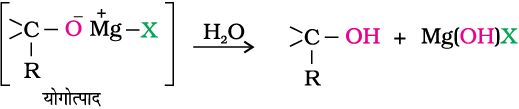
अभिक्रिया के प्रथम चरण में कार्बोनिल समूह पर ग्रीन्यार अभिकर्मक का नाभिकरागी संयोजन योगोत्पाद बनता है। योगोत्पाद के जल अपघटन से एेल्कोहॉल प्राप्त होती है।
 ... (i)
... (i)
 ... (ii)
... (ii)
विभिन्न एेल्डिहाइडों एवं कीटोनों की समग्र अभिक्रियाएं निम्नलिखित हैं–
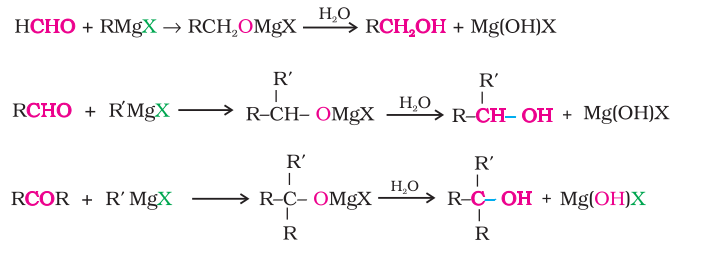
ग्रीन्यार अभिकर्मक की मेथेनैल द्वारा अभिक्रिया से प्राथमिक एेल्कोहॉल प्राप्त होती है, अन्य एेल्डिहाइड द्वितीयक एेल्कोहॉल तथा कीटोन तृतीयक एेल्कोहॉल देते हैं।
आप देख सकते हैं कि मेथेनैल के साथ प्राथमिक एेल्कोहॉल, किसी अन्य एेल्डिहाइड के साथ द्वितीयक एेल्कोहॉल तथा कीटोन के साथ तृतीयक एेल्कोहॉल प्राप्त होती हैं।
उदाहरण 11.2
निम्नलिखित अभिक्रियाओं के संभव उत्पादों की संरचनाएं तथा उनके आईयूपीएसी नाम दीजिए–
(क) ब्यूटेनैल का उत्प्रेरकी अपचयन
(ख) तनु सल्फ्यूरिक अम्ल की उपस्थिति में प्रोपीन का जलयोजन
(ग) प्रोपेनोन की मेथिलमैग्नीशियम ब्रोमाइड के साथ अभिक्रिया तत्पश्चात् जल अपघटन
(क) CH3–CH2–CH2–CH2–OH
(ख)  (ग)
(ग) 
ब्यूटेन-1-अॉल प्रोपेन-2-अॉल 2-मेथिलप्रोपेन-2-अॉल
11.4.2 फ़ीनॉलों का विरचन
फ़ीनॉल, जिसे कार्बोलिक अम्ल भी कहते हैं, का पृथक्करण सर्वप्रथम उन्नीसवीं शताब्दी के प्रारंभ में कोलतार से किया गया था। आजकलफ़ीनॉल का औद्योगिक उत्पादन संश्लेषण द्वारा किया जाता है। प्रयोगशाला मेंफ़ीनॉल को बेन्जीन के व्युत्पन्नों से निम्नलिखित में से किसी भी विधि से प्राप्त किया जा सकता है–
1. हैलोएेरीनों से
क्लोरोबेन्जीन को NaOH के साथ 623 K ताप एवं 320 वायुमंडलीय दाब पर संगलित किया जाता है। इस प्रकार प्राप्त सोडियमफ़ीनॉक्साइड का अम्लन करने परफ़ीनॉल प्राप्त होती है (एकक 10, कक्षा XII)।

विश्व मेंफ़ीनॉल का अधिकतर उत्पादन क्यूमीन से किया जाता है।
2. बेन्जीन सल्फोनिक अम्लों से
बेन्जीन का ओलियम द्वारा सल्फोनेशन किया जाता है तथा इससे प्राप्त सल्फोनिक अम्ल को गलित सोडियम हाइड्रॉक्साइड के साथ गरम करके सोडियमफ़ीनॉक्साइड में परिवर्तित कर लिया जाता है। सोडियम लवण के अम्लन सेफ़ीनॉल प्राप्त हो जाती है।

3. डाइएेज़ोनियम लवणों से
प्राथमिक एेरोमैटिक एेमीन की (273-278 K) ताप पर नाइट्रस अम्ल (NaNO2+HCl) के साथ अभिक्रिया द्वारा डाइएेज़ोनियम लवण बनते हैं। डाइएेज़ोनियम लवण जल के साथ गर्म करने पर अथवा तनु अम्लों के साथ क्रिया करने पर जल अपघटित हो जाते हैं औरफ़ीनाल देते हैं (एकक 13, कक्षा XII)।
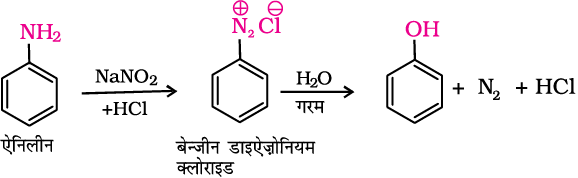
4. क्यूमीन से
फ़ीनॉल का उत्पादन हाइड्रोकार्बन क्यूमीन से किया जाता है। क्यूमीन (आइसोप्रोपिल बेन्जीन) को वायु की उपस्थिति में क्यूमीन हाइड्रोपरअॉक्साइड में अॉक्सीकृत कर लिया जाता है। तनु अम्ल के साथ क्रिया द्वारा इसेफ़ीनॉल तथा एेसीटोन में परिवर्तित किया जाता है। इस विधि से उत्पादन में इस अभिक्रिया का उपोत्पाद एेसीटोन भी अधिक मात्रा में प्राप्त होता है।
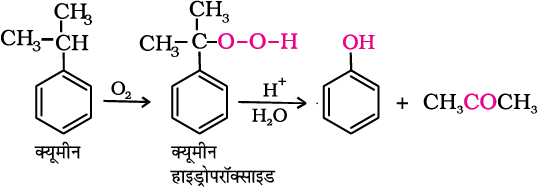
पाठ्यनिहित प्रश्न
11.4 दर्शाइए कि मेथेनैल पर उपयुक्त ग्रीन्यार अभिकर्मक से अभिक्रिया द्वारा निम्नलिखित एेल्कोहॉल कैसे विरचित किए जाते हैं?
(i) 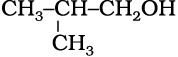 (ii)
(ii) 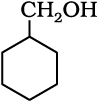
11.5 निम्नलिखित अभिक्रिया के उत्पादों की संरचना लिखिए–
(i) 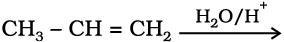 (iii)
(iii) 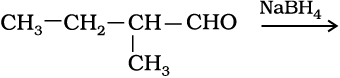
(ii) 
11.4.3 भौतिक गुणधर्म
एेल्कोहॉलों एवंफ़ीनॉलों के दो भाग होते हैं– एक एेल्किल/एेरिल समूह तथा दूसरा हाइड्रॉक्सिल समूह। एेल्कोहॉलों एवंफ़ीनॉलों के गुणधर्म मुख्यतः –OH समूह के कारण होते हैं। एेल्किल और एेरिल समूह की प्रकृति इन गुणधर्मों को सामान्यतः संशोधित करती हैं।


क्वथनांक
एेल्कोहॉलों और फ़ीनॉलों के क्वथनांक कार्बन परमाणुओं की संख्या में वृद्धि के साथ (वांडरवाल्स बलों में वृद्धि) बढ़ते हैैं। एेल्कोहॉलों में, शाखन के बढ़ने के साथ-साथ (पृष्ठ क्षेत्रफल घटने से वांडरवाल बलों में कमी के कारण) क्वथनांक कम हो जाते हैं।
एेल्कोहॉलों औरफ़ीनॉलों में –OH समूह अंतराआण्विक हाइड्रोजन आबंध बनाते हैं जैसा कि चित्रों में प्रदर्शित किया गया है।


यह रोचक तथ्य है कि लगभग समान आण्विक द्रव्यमान वाले अन्य वर्गों के यौगिकों यानी कि हाइड्रोकार्बनों, ईथरों और हैलोएेल्केनों हैलोएेरीनो के यौगिकों की तुलना में एेल्कोहॉलों तथाफ़ीनॉलों के क्वथनांक उच्चतर होते हैं। उदाहरणार्थ, एथेनॉल तथा प्रोपेन के आण्विक द्रव्यमान समतुल्य हैं किंतु इनके क्वथनांकों में काफ़ी अंतर है, मेथॉक्सीमेथेन का क्वथनांक इन दोनों के क्वथनांकों के मध्यवर्ती होता है।




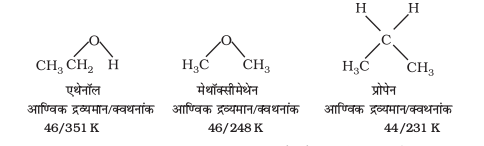
एेल्कोहॉलों के उच्च क्वथनांक मुख्यतः अंतराआण्विक हाइड्रोजन आबंध की उपस्थिति के कारण होते हैं जिसका ईथरों एवं हाइड्रोकार्बनों में अभाव है।
विलेयता
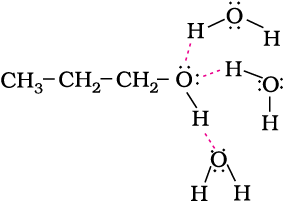
एेल्कोहॉलों औरफ़ीनॉलों की जल में विलेयता उनकी जल के अणुओं के साथ हाइड्रोजन आबंध बनाने की क्षमता के कारण होती है, जैसा कि चित्र में दिखाया गया है। यह विलेयता एेल्किल/एेरिल (जलविरागी) समूहों के आकार बढ़ने के साथ घटती है। अधिकांश निम्न आण्विक द्रव्यमान वाले एेल्कोहॉल जल में सभी अनुपातों में मिश्रणीय होते हैं।
उदाहरण 11.3
निम्नलिखित समूहों के यौगिकों को उनके क्वथनांकाें के बढ़ते हुए क्रम में व्यवस्थित
कीजिए-
(क) पेन्टेन-1-ऑल, ब्यूटेन-1-ऑल, ब्यूटेन-2-ऑल, एथेनॉल, प्रोपेन-1-ऑल, मेथेनॉल
(ख) पेन्टेन-1-ऑल, द-ब्यूटेन, पेन्टेनैल, एथॉक्सीएथेन
हल
(क) मेथेनॉल, एथेनॉल, प्रोपेन-1-ऑल, ब्यूटेन -2-ऑल, ब्यूटेन -1-ऑल, पेन्टेन-1-ऑल
(ख) द-ब्यूटेन, एथॉक्सीएथेन, पेन्टेनैल, पेन्टेन-1-ऑल
11.4.4 रासायनिक अभिक्रियाएँ
एेल्कोहॉल सर्वतोमुखी यौगिक हैं। ये नाभिकरागी (nucleophile) एवं इलेक्ट्रॉनरागी (electrophiles) दोनों के रूप में अभिक्रिया करती हैं।
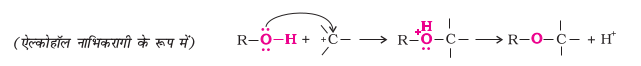
(i) जब एेल्कोहॉल नाभिकरागी के रूप में अभिक्रिया करती हैं तो O–H के मध्य आबंध टूटता है।
(ii) जब एेल्कोहॉल इलेक्टॉनरागी के रूप में अभिक्रिया करती है तो C-O के मध्य आबंध टूटता है। प्रोटॉनित एेल्कोहॉल इस प्रकार अभिक्रिया करती हैं–
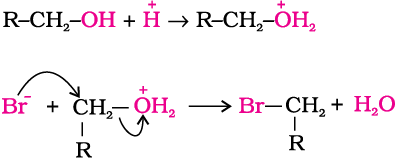
O–H व C–O आबंध के विदलन के आधार पर एेल्कोहॉलों एवंफ़ीनॉलों की अभिक्रिया को दो वर्गों में बाँटा जा सकता है–
(क) अभिक्रियाएँ जिनमें O–H आबंध का विदलन होता है
1. एेल्कोहॉलों एवंफ़ीनॉलों की अम्लता
(i) धातुओं के साथ अभिक्रियाएँ—
एेल्कोहॉल औरफ़ीनॉल सक्रिय धातुओं, जैसे— सोडियम, पोटैशियम तथा एेलुमिनियम के साथ अभिक्रिया करके संगत एेल्कॉक्साइड/फ़ीनॉक्साइड एवं हाइड्रोजन देती हैं।
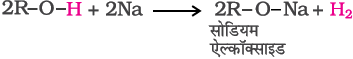
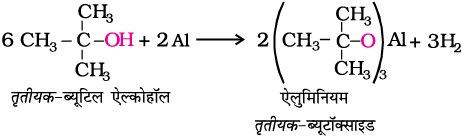

इसके अतिरिक्त फ़ीनॉल जलीय सोडियम हाइड्रॉक्साइड के साथ अभिक्रिया द्वारा सोडियमफ़ीनॉक्साइड बनाती हैं।

उपरोक्त अभिक्रियाएं दर्शाती हैं कि एेल्कोहॉल एवंफ़ीनॉल अम्लीय प्रकृति की होती हैं। वास्तव में, एेल्कोहॉल एवंफ़ीनॉल ब्रंसटेद अम्ल है अर्थात् वे किसी प्रबल क्षारक (B:) को प्रोटॉन प्रदान कर सकती हैं।
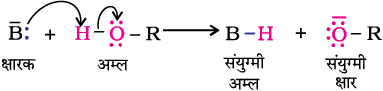
(ii) एेल्कोहॉलों की अम्लता–
एेल्कोहॉलों की अम्लीय प्रकृति ध्रुवीय O-H आबंध के कारण होती है इलेक्ट्रॉन विमोचक (दाता) समूह (–CH3, –C2H5) अॉक्सीजन परमाणु पर इलेक्ट्रॉन घनत्व बढ़ा देते हैं जिससे O–H आबंध की ध्रुवता कम हो जाती है इससे अम्ल सामर्थ्य कम हो जाती है। इसके कारण एेल्कोहॉलों की अम्ल-सामर्थ्य निम्नलिखित क्रम में घटती है–
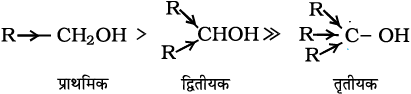
एेल्कोहॉल जल की अपेक्षा दुर्बल अम्ल होती हैं। जल की एेल्कॉक्साइड से अभिक्रिया कराने पर यह स्पष्ट हो जाता है।
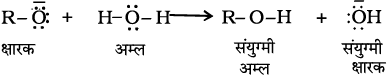
यह अभिक्रिया प्रदर्शित करती है कि एेल्कोहॉल की अपेक्षा जल एक बेहतर प्रोटॉन दाता है। (यानी कि प्रबलतर अम्ल), उपरोक्त अभिक्रिया में हम यह भी देख सकते हैं कि एक एेल्कॉक्साइड आयन हाइड्रॉक्साइड आयन की अपेक्षा एक बेहतर प्रोटॉनग्राही होता है। जो यह संकेत देता है कि एेल्कॉक्साइड प्रबलतर क्षारक होते हैं। (सोडियम एथॉक्साइड, सोडियम हाइड्रॉक्साइड से अधिक क्षारीय होता है।)
एेल्कोहॉल भी ब्रंसटेद क्षारकों की भाँति कार्य करते हैं। एेसा अॉक्सीजन पर उपस्थित असहभाजित इलेक्ट्रॉन युगलों के कारण होता है जो इन्हें प्रोटॉनग्राही बनाते हैं।
(iii)फ़ीनॉलों की अम्लता—
फ़ीनॉल की धातुओं (उदाहरणार्थ; सोडियम तथा एेलुमिनियम) तथा सोडियम हाइड्रॉक्साइड के साथ अभिक्रियाएं इसकी अम्लीय प्रकृति को दर्शाती हैं।फ़ीनॉल में हाइड्रॉक्सिल समूह बेन्जीन वलय के sp2 संकरित कार्बन से सीधा संयुक्त रहता है जो कि इलेक्ट्रॉन अपनयक समूह के रूप में कार्य करता है। इसके कारणफ़ीनॉल अणु में आवेश वितरण से –OH समूह की अॉक्सीजन धनावेशित हो जाती है जैसा कि अनुनादी संरचनाओं द्वारा चित्रित किया गया है।
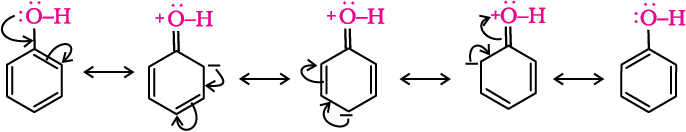
एेस्पिरिन, पीड़ाहारी, शोथनाशी एवं ज्वरनाशी गुणधर्म वाली होती है।
फ़ीनॉल की जलीय सोडियम हाइड्रॉक्साइड के साथ अभिक्रिया यह इंगित करती है किफ़ीनॉल, एेल्कोहॉलों तथा जल की अपेक्षा अधिक प्रबल अम्ल होती हैं। आइए, यह जाँचें कि एेरोमैटिक वलय से जुड़ा हाइड्रॉक्सिल समूह, एेल्किल समूह से जुड़े हाइड्रॉक्सिल समूह की अपेक्षा अधिक अम्लीय कैसे हो जाता है।
किसी एेल्कोहॉल तथाफ़ीनॉल का आयनन निम्नलिखित प्रकार से होता है।
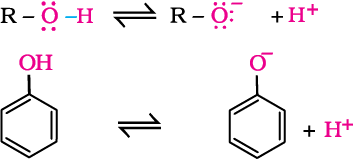
फ़ीनॉल में –OH से संयुक्त sp2 संकरित कार्बन की उच्च विद्युतऋणात्मकता के कारण अॉक्सीजन पर इलेक्ट्रॉन घनत्व कम हो जाता है जिससे O–H आबंध की ध्रुवता बढ़ती है, जिसके फलस्वरूप एेल्कोहॉल की अपेक्षाफ़ीनॉल के आयनन में वृद्धि होती है। अब, हम एेल्कॉक्साइड एवंफ़ीनॉक्साइड आयनों के स्थायित्व के बारे में जाँच करें। एेल्कॉक्साइड आयनों में ऋणावेश अॉक्सीजन पर स्थानागत होता है जबकिफ़ीनॉक्साइड आयनों में विस्थानित होता है। ऋणावेश का विस्थानन (संरचना I-V) फ़ीनॉक्साइड आयनों को अधिक स्थायी बनाता है तथाफ़ीनॉल के आयनन में सहायक होता है। यद्यपिफ़ीनॉल में भी आवेश का विस्थानन होता है परंतु इसकी अनुनादी संरचनाओं में आवेशों का पृथकन होता है जिसके कारणफ़ीनॉक्साइड आयन की अपेक्षाफ़ीनॉल अणु कम स्थायी होता है।

प्रतिस्थापित फ़ीनॉलों में नाइट्रो समूह जैसे इलेक्ट्रॉन अपनयक (प्रत्याहार्य) समूह, फ़ीनॉल की अम्लीय सामर्थ्य को बढ़ा देते हैं। जब एेसे समूह अॉर्थो एवं पैरा स्थितियों पर उपस्थित होते हैं तो यह प्रभाव अधिक प्रबल हो जाता है। इसका कारणफ़ीनॉक्साइड आयन के आर्थो एवं पैरा स्थान पर के ऋणावेश का प्रभावी विस्थानन होता है। दूसरी ओर एेल्किल समूह जैसे इलेक्ट्रॉन विमोचक (दाता) समूह सामान्य रूप से फ़ीनॉक्साइड आयन के बनने में सहायक नहीं होते, परिणामस्वरूप अम्ल सामर्थ्य में कमी आ जाती है। उदाहरणार्थ;फ़ीनॉल की अपेक्षा क्रीसॉल कम अम्लीय होते हैं।
उपरोक्त आँकड़ों के आधार पर आप देखेंगे कि फ़ीनॉल एथेनॉल की तुलना में दस लाख गुना अधिक अम्लीय है।
सारणी 11.3– कुछफ़ीनॉलों और एेथेनॉल के pKa का मान
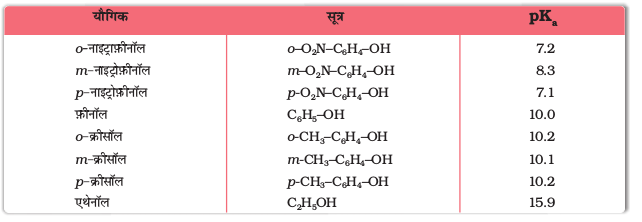
pKa मान जितना अधिक होगा, अम्ल उतना ही दुर्बल होगा।
2. एस्टरीकरण
एेल्कोहॉल एवं फ़ीनॉल कार्बाक्सिलिक अम्लों, अम्ल क्लोराइडों एवं अम्ल एेनहाइड्राइडों के साथ अभिक्रिया द्वारा एस्टर बनाती हैं।



कार्बाक्सिलिक अम्ल तथा अम्ल एेनहाइड्राइड की अभिक्रिया सांद्र सल्फ्यूरिक अम्ल की कुछ मात्रा की उपस्थिति में संपन्न होती है। यह अभिक्रिया उत्क्रमणीय होती है, अतः इसमें बने जल को तुरंत निष्कासित कर दिया जाता है। अम्ल क्लोराइड के साथ अभिक्रिया क्षारक (पिरिडीन) की उपस्थिति में की जाती है जिससे कि अभिक्रिया से बने HCl को उदासीन किया जा सके। यह साम्य को दाईं ओर विस्थापित कर देता है। एेल्कोहॉल तथाफ़ीनॉल में एेसीटिल (CH3CO) समूह का प्रवेश एेसीटिलन कहलाता है। एेस्पिरिन सैलिसिलिक अम्ल के एेसीटिलन से प्राप्त होती है।
तृतीयक कार्बोकैटायन अधिक स्थायी होते हैं, अतः द्वितीयक एवं तृतीयक कार्बोकैटायनों की अपेक्षा आसानी से बनते हैं। तृतीयक एेल्कोहॉलों का निर्जलन करना सबसे अधिक आसान है।
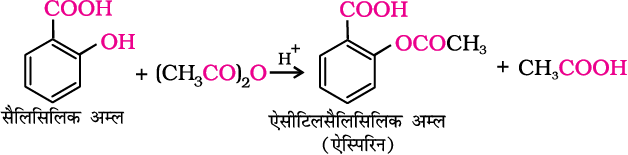
(ख) अभिक्रियाएँ जिनमें कार्बन-अॉक्सीजन (C–O) आबंध का विदलन (Cleavage) होता है
C–O आबंध विदलन की अभिक्रियाएँ केवल एेल्कोहॉलों में पाई जाती हैं।फ़ीनॉल इस प्रकार की अभिक्रिया केवल जस्त चूर्ण के साथ प्रदर्शित करती हैं।
1. हाइड्रोजन हैलाइडों के साथ अभिक्रिया
एेल्कोहॉल, हाइड्रोजन हैलाइडों के साथ अभिक्रिया करके एेल्किल हैलाइड बनाती हैं (देखिए- एकक 10, कक्षा XII)
ROH + HX → R–X + H2O
इन तीनों वर्गों की एेल्कोहॉलों की HCl के प्रति अभिक्रियाशीलता के आधार पर इनमें विभेद किया जा सकता है (ल्यूकास परीक्षण)। एेल्कोहॉल ल्यूकास अभिकर्मक (सांद्र HCl एवं ZnCl2) में विलेय होती हैं जबकि उनके हैलाइड अमिश्रणीय होते हैं तथा विलयन में धुुँधलापन (आविलता) उत्पन्न कर देते हैं। तृतीयक एेल्कोहॉलों द्वारा धुुँधलापन तत्काल उत्पन्न हो जाता है; क्योंकि वे आसानी से हैलाइड बनाती हैं। प्राथमिक एेल्कोहॉल सामान्य ताप पर धुुँधलापन उत्पन्न नहीं करतीं।
2. फ़ॉस्फ़ोरस ट्राइहैलाइडों के साथ अभिक्रिया
फ़ॉस्फ़ोरस ट्राइब्रोमाइड के साथ अभिक्रिया करने पर एेल्कोहॉल, एेल्किल ब्रोमाइड में परिवर्तित हो जाती है (देखिए— एकक 10, कक्षा XII)।
3. निर्जलन
एेल्कोहॉल के सांद्र H2SO4 या H3PO4 जैसे प्रोटिक अम्लों अथवा निर्जलितज़िंक क्लोराइड एेलुमिना जैसे उत्प्रेरकों के द्वारा निर्जलित होने (जल के अणु के निष्कासन) पर एेल्कीन बनती हैं (एकक 13, कक्षा XI)।
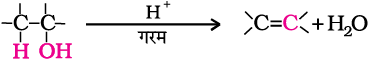
443 K ताप पर सांद्र H2SO4 के साथ गरम करने पर एथेनॉल का निर्जलन हो जाता है।
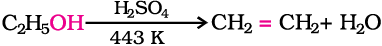
द्वितीयक तथा तृतीयक एेल्कोहॉलों का निर्जलन अपेक्षाकृत मध्यम परिस्थितियों में किया जाता है। उदाहरणार्थ–
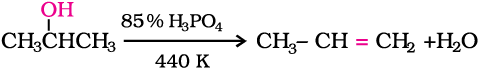
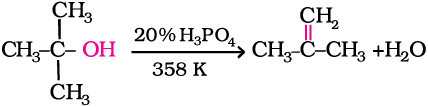
एेल्कोहॉलों के सापेक्षिक निर्जलन की सुगमता का क्रम इस प्रकार होता है–
तृतीयक > द्वितीयक > प्राथमिक
एथेनॉल के निर्जलन की क्रियाविधि में निम्नलिखित चरण होते हैं–
क्रियाविधि
चरण 1–
प्रोटॉनित एेल्कोहॉल का बनना–

चरण 2–
कार्बोकैटायन का बनना–
यह सबसे धीमा चरण है अतः यह अभिक्रिया का दर निर्धारक चरण होता है।
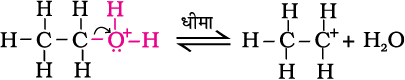
चरण 3–
प्रोटॉन के निकल जाने से एथीन का बनना–
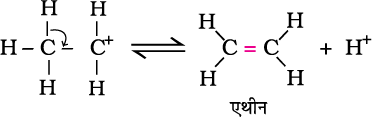
मेथेनॉल एवं एथेनॉल के जैविक अॉक्सीकरण से शरीर में संगत एेल्डिहाइड बनते हैं, तत्पश्चात् अम्ल बनते हैं। कभी-कभी मद्यव्यसनी गलती से मेथेनॉल मिश्रित एेथेनॉल जिसे विगुणित एेल्कोहॉल भी कहते हैं, पी लेते हैं। शरीर में मेथेनॉल पहले मेथेनैल में अॉक्सीकृत होती है; तत्पश्चात् मेथेनॉइक अम्ल में, जो कि अन्धता एवं मृत्यु का कारण बन सकता है। मेथेनॉल की विषाक्तता के रोगी का उपचार तनुकृत एेथेनॉल को अंतः शिरा द्वारा प्रदान करके किया जाता है। एेल्डीहाइड (HCHO) को अम्ल में अॉक्सीकृत करने के लिए उत्तरदायी एन्जाइम जल ग्रहण कर लेता है जिससे वृक्क को मेथेनॉल उत्सर्जित करने के लिए समय प्राप्त हो जाता है।
चरण 1 में प्रयुक्त अम्ल, अभिक्रिया के चरण 3 में मुक्त हो जाता है। साम्य को दाईं ओर विस्थापित करने के लिए, एथीन बनते ही निष्कासित कर ली जाती है।
4. अॉक्सीकरण–
एेल्कोहॉलों के अॉक्सीकरण में O–H एवं C–H आबंधों का विदलन होता है तथा कार्बन-अॉक्सीजन द्विआबंध बनता है।

आबंधों का एेसा विदलन एवं निर्माण अॉक्सीकरण अभिक्रियाओं में होता है। इन्हें विहाइड्रोजनन अभिक्रियाएं भी कहते हैं क्योंकि इनमें एेल्कोहॉल अणु में से डाइहाइड्रोजन अणु की कमी हो जाती है। प्रयुक्त अॉक्सीकरण कर्मक के आधार पर, प्राथमिक एेल्कोहॉल, एेल्डिहाइड में अॉक्सीकृत हो जाती हैं जो बाद में कार्बोक्सिलिक अम्ल में अॉक्सीकृत हो जाता है।
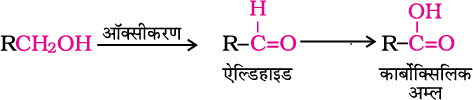
एेल्कोहॉलों से सीधे कार्बोक्सिलिक अम्लों को प्राप्त करने के लिए प्रबल अॉक्सीकरण कर्मकों, जैसे अम्लीकृत पोटैशियम परमैंगनेट का उपयोग किया जाता है। एेल्डिहाइडों को पृथक् करने के लिए CrO3 का निर्जल माध्यम में अॉक्सीकरण कर्मक की तरह उपयोग किया जाता है।
2,4,6-ट्राइनाइट्रोफ़ीनॉल तीन इलेक्ट्रॉन अपनयक –NO2 समूहों की उपस्थिति के कारण प्रबल अम्ल होती है। यह समूह हाइड्रोजन आयन निकलने में सहायक होते हैं।
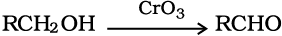
प्राथमिक एेल्कोहॉल के अॉक्सीकरण से एेल्डिहाइड की अच्छी लब्धि प्राप्त करने के लिए पिरिडीनियम क्लोरोक्रोमेट (PCC) श्रेष्ठ अभिकर्मक है जो कि क्रोमियम ट्राइअॉक्साइड का पिरिडीन व HCl के साथ संकुल है।
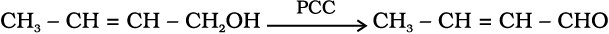
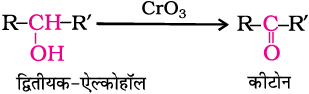
द्वितीयक एेल्कोहॉल क्रोमिक एेनहाइड्राइड (CrO3) द्वारा कीटोनों में अॉक्सीकृत हो जाती हैं।
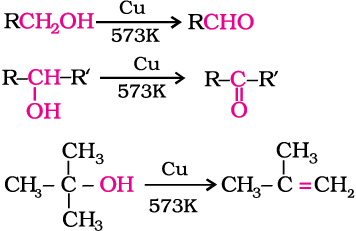
तृतीयक एेल्कोहॉल अॉक्सीकरण अभिक्रिया नहीं करते। प्रबल अभिक्रिया परिस्थितियों, जैसे– प्रबल आक्सीकरण कर्मकों (KMnO4) एवं उच्च ताप पर विभिन्न C–C आबंधों का विदलन होता है। जिससे कार्बोक्सिलिक अम्लों का मिश्रण प्राप्त होता है जिनमें कार्बन परमाणुओं की संख्या कम होती है।
जब प्राथमिक अथवा द्वितीयक एेल्कोहॉल के वाष्पों को 573 K पर तप्त कॉपर के ऊपर से प्रवाहित किया जाता है तो विहाइड्रोजनन होता है तथा एेल्डिहाइड अथवा कीटोन बनते हैं। जबकि तृतीयक एेल्कोहॉलों का निर्जलन होता है।
मेथेनॉल एवं एथेनॉल के जैविक ऑक्सीकरण से शरीर में संगत ऐल्डिहाइड बनते हैं, तत्पश्चात् अम्ल बनते हैं। कभी-कभी मद्यव्यसनी गलती से मेथेनॉल मिश्रित ऐथेनॉल जिसे विगुणित ऐल्कोहॉल भी कहते हैं, पी लेते हैं। शरीर में मेथेनॉल पहले मेथेनैल में ऑक्सीकृत होती है_ तत्पश्चात् मेथेनॉइक अम्ल में, जो कि अन्धता एवं मृत्यु का कारण बन सकता है। मेथेनॉल की विषाक्तता के रोगी का उपचार तनुकृत ऐथेनॉल को अंतः शिरा द्वारा प्रदान करके किया जाता है। ऐल्डीहाइड (HCHO) को अम्ल में ऑक्सीकृत करने के लिए उत्तरदायी एन्जाइम जल ग्रहण कर लेता है जिससे वृक्क को मेथेनॉल उत्सर्जित करने के लिए समय प्राप्त हो जाता है।
(ग)फ़ीनॉल की अभिक्रियाएँ
निम्नलिखित अभिक्रियाएँ केवलफ़ीनालों द्वारा दर्शायी जाती हैं–
1. एेरोमैटिक इलेक्ट्रॉनरागी प्रतिस्थापन–
फ़ीनॉलों में एेरोमैटिक वलय पर होने वाली अभिक्रियाएँ इलेक्ट्रॉनरागी प्रतिस्थापन अभिक्रियाएँ होती हैं। (एकक 13, कक्षा XI)। बेन्जीन वलय पर जुड़ा –OH समूह इसे इलेक्ट्रॉनरागी प्रतिस्थापन अभिक्रिया की ओर सक्रियित करता है और आने वाले समूह को वलय में अॉर्थो एवं पैरा स्थिति पर निर्दिष्ट करता है। जिससे –OH समूह के अनुनाद प्रभाव के कारण ये स्थितियाँ इलेक्ट्रॉन-धनी हो जाती हैं। इनकी अनुनादी संरचनाएँ फ़ीनॉलों की अम्लता शीर्षक के अंतर्गत दर्शायी गई हैं।
फ़ीनॉलों की सामान्य इलेक्ट्रॉनरागी एेरोमैटिक प्रतिस्थापन अभिक्रियाएँ निम्नलिखित हैं–
(i) नाइट्रोकरण
निम्न ताप (298 K) पर तनु नाइट्रिक अम्ल के साथफ़ीनॉल के नाइट्रोकरण से अॉर्थो-नाइट्रोफ़ीनॉल एवं पैरा नाइट्रोफ़ीनॉल का मिश्रण प्राप्त होता है।

अॉर्थो एवं पैरा समावयवों को वाष्पीय आसवन द्वारा पृथक् किया जा सकता है। आंतरआण्विक हाइड्रोजन आबंध के कारण अॉर्थो-नाइट्रोफ़ीनॉल भाप द्वारा वाष्पित होती है जबकि पैरा-नाइट्रोफ़ीनॉल कम वाष्पशील होती है क्योंकि इसमें अंतराआण्विक हाइड्रोजन आबंध विद्यमान होता है, जिससे अणु संगुणित हो जाते हैं।
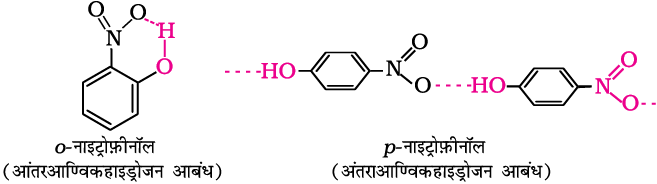
सांद्र नाइट्रिक अम्ल के साथफ़ीनॉल 2,4,6-ट्राइनाइट्रोफ़ीनॉल में परिवर्तित हो जाती है। उत्पाद को सामान्यतः पिक्रिक अम्ल कहते हैं। अभिक्रिया उत्पाद की लब्धि बहुत कम होती है।
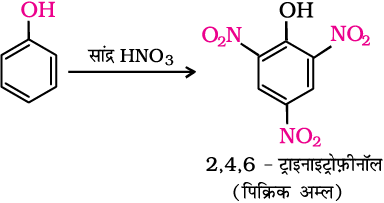
उदाहरण 11.5
हल निम्नलिखित अभिक्रियाओं से बनने वाले मुख्य उत्पादों की संरचनाएं दीजिए।
(क) 3-मेथिलफ़ीनॉल का मोनोनाइट्रोकरण
(ख) 3-मेथिलफ़ीनॉल का डाइनाइट्रोकरण
(ग) फ़ेनिलएेथेनोएट का मोनोनाइट्रोकरण
–OH और –CH3 समूहों का संयुक्त प्रभाव प्रवेश करने वाले समूहों की स्थिति निर्धारित करता है।
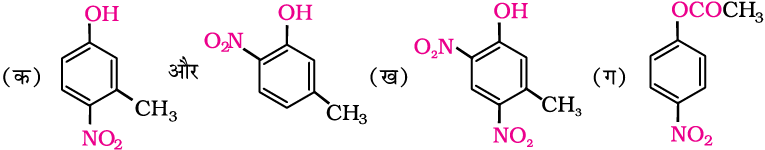
पाठ्यनिहित प्रश्न
11.6 यदि निम्नलिखित एेल्कोहॉल क्रमशः (क) HCl–ZnCl2 (ख) HBr (ग) SOCl2 से अभिक्रिया करें तो आप अपेक्षित उत्पादों की संरचनाएं दीजिए।
(i) ब्यूटेन -1-अॉल (ii) 2-मेथिलब्यूटेन-2-अॉल
11.7 (i) 1-मेथिलसाइक्लोहैक्सेनॉल और (ii) ब्यूटेन-1-अॉल के अम्ल उत्प्रेरित निर्जलन के मुख्य उत्पादों की प्रागुक्ति कीजिए।
11.8 अॉर्थो तथा पैरा नाइट्रोफ़ीनॉल,फ़ीनॉल से अधिक अम्लीय होती हैं। उनके संगतफ़ीनॉक्साइड आयनों की अनुनादी संरचनाएं बनाइए।
11.9 निम्नलिखित अभिक्रियाओं में सम्मिलित समीकरण लिखिए–
(i) राइमर-टीमन अभिक्रिया (ii) कोल्बे अभिक्रिया
आजकल पिक्रिक अम्ल को बनाने के लिए सर्वप्रथम फ़ीनॉल की अभिक्रिया
सांद्र H2SO4 के साथ करते हैं जिससे यहफ़ीनॉल-
2, 4-डाइसल्फ़ोनिक अम्ल में परिवर्तित हो जाती है। तत्पश्चात् सांद्रHNO3 के साथ अभिक्रिया द्वारा 2,4,6 - ट्राइनाइट्रोफ़ीनॉल प्राप्त कर लेते हैं।
क्या आप इसमें सम्मिलित अभिक्रियाओं का समीकरण लिख सकते हैं?
(ii) हैलोजनन
फ़ीनॉल की ब्रोमीन के साथ अभिक्रिया द्वारा अलग-अलग प्रायोगिक अवस्थाओं में अलग-अलग उत्पाद प्राप्त होते हैं।
(क) जब CHCl3 अथवा CS2 जैसे कम ध्रुवीय विलायकों में निम्न ताप पर अभिक्रिया की जाती है तो मोनोब्रोमोफ़ीनॉल प्राप्त होती है।
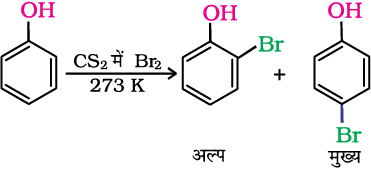
बेन्जीन का सामान्य हैलोजनन FeBr3 जैसे लूइस अम्ल की उपस्थिति में होता है (एकक 10, कक्षा XII), जो हैलोजन अणु को ध्रुवित कर देता है।फ़ीनॉल की अभिक्रिया में ब्रोमीन का ध्रुवण लूइस अम्ल की अनुपस्थिति में भी संभव होता है। इसका कारण बेन्जीन से जुड़े –OH समूह का वलय पर उच्च सक्रियण प्रभाव होता है।
(ख) जबफ़ीनॉल की अभिक्रिया ब्रोमीन जल के साथ की जाती है तो 2,4,6-ट्राइब्रोमोफ़ीनॉल श्वेत अवक्षेप के रूप में बनता है।
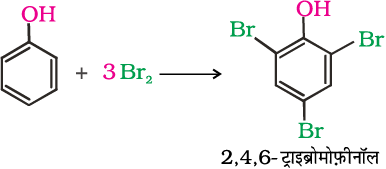
2. कोल्बे अभिक्रिया
फ़ीनॉल को सोडियम हाइड्रॉक्साइड के साथ अभिकृत कराने से बनाफ़ीनॉक्साइड आयन, फ़ीनॉल की अपेक्षा इलेक्ट्रॉनरागी एेरोमैटिक प्रतिस्थापन अभिक्रिया के प्रति अधिक क्रियाशील होता है। अतः यह CO2 जैसे दुर्बल इलेक्ट्रॉनरागी के साथ इलेक्ट्रॉनरागी प्रतिस्थापन अभिक्रिया करता है। इससे अॉर्थो हाइड्रॉक्सीबेन्ज़ोइक अम्ल मुख्य उत्पाद के रूप में प्राप्त होता है।

3. राइमर-टीमन अभिक्रिया
फ़ीनॉल की सोडियम हाइड्रॉक्साइड की उपस्थिति में क्लोरोफ़ार्म के साथ अभिक्रिया से बेन्जीन में, –CHO समूह अॉर्थो स्थिति पर प्रवेश कर जाता है। इस अभिक्रिया को राइमर-टीमन अभिक्रिया (Reimer-Tiemann reaction) कहते हैं।
प्रतिस्थापित मध्यवर्ती बेन्ज़िल क्लोराइड क्षार की उपस्थिति में अपघटित होकर सैलिसैल्डिहाइड बनाता है।

4.फ़ीनॉल की यशदरज के साथ अभिक्रिया
यशदरज के साथ गरम करने परफ़ीनॉल बेन्जीन में परिवर्तित हो जाती है।
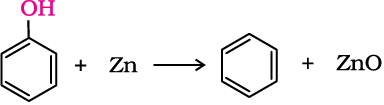
5. आक्सीकरण
फ़ीनॉल के क्रोमिक अम्ल द्वारा आक्सीकरण से संयुग्मित डाइकीटोन बनता है जिसे बेन्ज़ोक्विनोन कहते हैं। वायु की उपस्थिति मेंफ़ीनॉल धीरे-धीरे गहरे रंग के क्विनोनों के मिश्रण में अॉक्सीकृत हो जाते हैं।
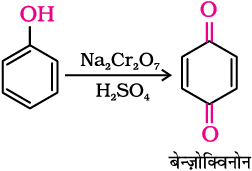
पाठ्यनिहित प्रश्न
11.6 यदि निम्नलिखित ऐल्कोहॉल क्रमशः (क) HCl–ZnCl2 (ख) HBr (ग)SOCl2 से अभिक्रिया करें तो आप अपेक्षित उत्पादों की संरचनाएं दीजिए।
(i) ब्यूटेन -1-ऑल (ii) 2-मेथिलब्यूटेन-2-ऑल
11.7 (i) 1-मेथिलसाइक्लोहैक्सेनॉल और (ii) ब्यूटेन-1-ऑल के अम्ल उत्प्रेरित निर्जलन के मुख्य उत्पादों की प्रागुक्ति कीजिए।
11.8 ऑर्थो तथा पैरा नाइट्रोप़्ाफ़ीनॉल, प़्ाफ़ीनॉल से अधिक अम्लीय होती हैं। उनके संगत प़्ाफ़ीनॉक्साइड आयनों की अनुनादी संरचनाएं बनाइए।
11.9 निम्नलिखित अभिक्रियाओं में सम्मिलित समीकरण लिखिए-
(i) राइमर-टीमन अभिक्रिया (ii) कोल्बे अभिक्रिया
११.५ औोगिक महत्व के कुछ एेल्कोहॉल
मेथेनॉल एवं एथेनॉल दो औद्योगिक महत्व की एेल्कोहॉल हैं।
1. मेथेनॉल
मेथेनॉल, CH3OH जिसे ‘काष्ठ स्प्रिट’ भी कहते हैं, लकड़ी के भंजक आसवन द्वारा प्राप्त की जाती थी। वर्तमान में अधिकांश मेथेनॉल का उत्पादन उच्च ताप एवं दाब पर
ZnO – Cr2O3 उत्प्रेरक की उपस्थिति में कार्बन मोनोक्साइड के उत्प्रेरकी हाइड्रोजनन द्वारा किया जाता है।

मेथेनॉल एक रंगहीन द्रव है, जिसका क्वथनांक 337 K होता है। यह अत्यंत विषैली प्रकृति की होती है। इसके बहुत कम मात्रा में सेवन से भी अंधापन हो सकता है और
इसकी अधिक मात्रा से मृत्यु भी हो सकती है। मेथेनॉल का उपयोग पेंट और वार्निश के लिए विलायक के रूप में और मुख्य रूप से फॉर्मेल्डीहाइड को बनाने के लिए किया जाता है।
2. एथेनॉल
एथेनॉल के सेवन का प्रभाव केंद्रीय तंत्रिका तंत्र पर पड़ता है। मध्यम मात्रा में यह निर्णय क्षमता पर प्रभाव डालती है तथा अंतर्बाधा को कम करती है। अधिक सांद्रता मितली और बेहोशी लाती है। उच्च सांद्रताओं में यह स्वतः श्वसन क्रिया में भी बाधा डालती है और प्राणघातक हो सकती है।
एेथेनॉल C2H5 OH को औद्योगिक स्तर पर किण्वन द्वारा प्राप्त किया जाता है। शर्करा के किण्वन से एथेनॉल प्राप्त करने की यह विधि सबसे पुरानी है। मोलैसेज (शीरे), गन्ने अथवा अंगूर जैसे फलों की शर्करा को इनवर्टेस एन्जाइम की उपस्थिति में ग्लूकोस एवं फ्रक्टोज़ (दोनों का आण्विक सूत्र C6H12O6 है) में परिवर्तित कर लिया जाता है। ग्लूकोस एवं फ्रक्टोज़ को यीस्ट में पाए जाने वाले दूसरे एन्जाइम जाइमेज द्वारा किण्वन किया जाता है।
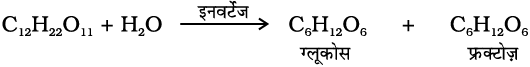
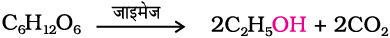
शराब बनाने के लिए अंगूर शर्करा (द्राक्ष-शर्करा) तथा यीस्ट का स्रोत होते हैं। जब अंगूर पक जाते हैं तो उनमें शर्करा की मात्रा बढ़ जाती है तथा उनकी ऊपरी सतह पर यीस्ट उत्पन्न हो जाती है। जब अंगूरों को कुचला जाता है तो शर्करा एवं एन्जाइम संपर्क में आते हैं तथा किण्वन आरंभ हो जाता है। किण्वन अवायवीय स्थितियों यानी कि वायु की अनुपस्थिति में होता है। किण्वन में कार्बनडाइअॉक्साइड निर्मुक्त होती है।
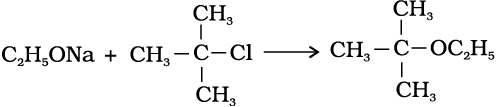
उदाहरण 11.6 निम्नलिखित अभिक्रिया तृतीयक ब्यूटिल एथिल ईथर बनाने के लिए उपयुक्त नहीं है।
हल
(i) इस अभिक्रिया का मुख्य उत्पाद क्या होगा?
(ii) तृतीयक-ब्यूटिलएथिल ईथर बनाने के लिए उपयुक्त अभिक्रिया लिखिए?
(i) दी गई अभिक्रिया में 2-मेथिलप्रोप-1-ईन मुख्य उत्पाद है; क्योंकि सोडियम एथॉक्साइड एक प्रबल नाभिकरागी एवं प्रबल क्षारक है, अतः विलोपन प्रतिस्थापन से अधिक प्रधान होता है।
(ii) 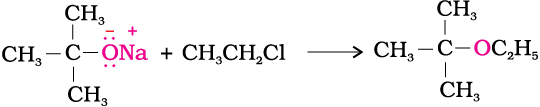
उत्पन्न एेल्कोहॉल की मात्रा 14% से अधिक हो जाने पर जाइमेज की क्रिया संदमित हो जाती है। यदि किण्वन मिश्रण में वायु आ जाती है तो वायु की अॉक्सीजन एथेनॉल को एथेनोइक अम्ल में आक्सीकृत कर देती है, जिससे एेल्कोहॉली पेय का स्वाद नष्ट हो जाता है।
एथेनॉल एक रंगहीन द्रव है, जिसका क्वथनांक 351 K है। यह पेंट उद्योग में विलायक के रूप में तथा कार्बन के अनेक यौगिकों के विरचन में प्रयुक्त की जाती है। औद्योगिक एेल्कोहॉल (सामान्य एथेनॉल) को कुछ कॉपर सल्फेट (रंग प्रदान करने के लिए) एवं पिरिडीन (दुर्गंधयुक्त तरल) मिलाकर पीने के अयोग्य बना दिया जाता है। इस प्रक्रम को एेल्कोहॉल का विकृतीकरण कहते हैं। आजकल एथेनॉल की अधिक मात्रा एथीन के जलयोजन द्वारा प्राप्त की जाती है (खंड 11.4)।
११.६ ईथर
डाइएथिल ईथर का उपयोग अंतःश्वसन निश्चेतक के रूप में होता रहा है। परंतु इसके धीमे असर एवं अप्रिय स्वास्थ्यलाभ समय के कारण, इसका प्रतिस्थापन दूसरे यौगिकों द्वारा कर दिया गया है।
11.6.1 ईथरों का विरचन
1. एेल्कोहॉलों के निर्जलन द्वारा
प्रोटिक अम्लों (H2SO4, H3PO4) की उपस्थिति में एेल्कोहॉल निर्जलित हो जाती है। अभिक्रिया का उत्पाद एेल्कीन होगा अथवा ईथर; यह अभिक्रिया की परिस्थितियों पर निर्भर करता है। उदाहरणार्थ; 443 K ताप पर सल्फ्यूरिक अम्ल की उपस्थिति में एथेनॉल निर्जलित होकर एथीन देती है। 413 K ताप पर एथॉक्सीएथेन मुख्य उत्पाद होता है।
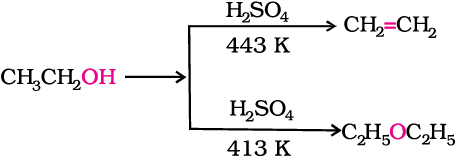
ईथर का विरचन एक द्विअणुक नाभिकरागी प्रतिस्थापन अभिक्रिया (SN2 अभिक्रिया) है जिसमें एेल्कोहॉल अणु एक प्रोटॉनित एेल्कोहॉल अणु पर आक्रमण करता है जैसा कि नीचे दर्शाया गया है–
(i) 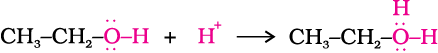
(ii)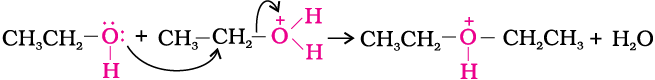
(iii) 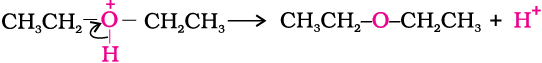
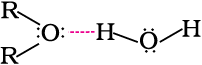
एेल्कोहॉलों का अम्लीय निर्जलन, जिसमें एेल्कीन बनती है, एक प्रतिस्थापन अभिक्रिया से भी संबंधित है जो ईथर देती है।
यह विधि केवल प्राथमिक एेल्किल समूह युक्त ईथरों के विरचन के लिए ही उपयुक्त होती है। एेल्किल समूह अबाधित तथा तापक्रम निम्न होना चाहिए अन्यथा अभिक्रिया एेल्कीन के बनने में सहायक होगी। जब एेल्कोहॉल द्वितीयक या तृतीयक होती है तो अभिक्रिया SN1 पथ का अनुसरण करती है, जिसके बारे में आप उच्च कक्षाओं में अध्ययन करेंगे। तथापि द्वितीयक और तृतीयक एेल्कोहॉलों के निर्जलन से ईथरों को प्राप्त करना असफल होता है; क्योंकि प्रतिस्थापन और विलोपन की प्रतिस्पर्धा में प्रतिस्थापन की बजाय विलोपन होने के परिणामस्वरूप एेल्कीनें सरलता से बनती हैं।
क्या आप समझा सकते हैं कि द्विअणुक निर्जलन, एथिल मेथिल ईथर के विरचन के लिए उपयुक्त क्यों नहीं है?
2. विलियम्सन संश्लेषण
यह सममित और असममित ईथरों को बनाने की एक महत्वपूर्ण प्रयोगशाला विधि है। इस विधि में, एेल्किल हैलाइड की सोडियम एेल्कॉक्साइड के साथ अभिक्रिया कराई जाती है।

प्रतिस्थापित (द्वितीयक अथवा तृतीयक) एेल्किल समूह युक्त ईथर भी इस विधि द्वारा बनाई जा सकती हैं। इस अभिक्रिया में प्राथमिक एेल्किल हैलाइड पर एेल्कॉक्साइड आयन का (SN2) आक्रमण होता है।
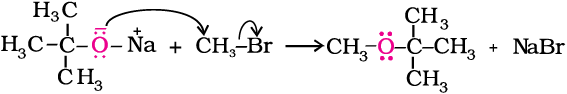
अगर एेल्किल हैलाइड प्राथमिक होता है तो अच्छे परिणाम प्राप्त होते हैं। द्वितीयक एवं तृतीयक एेल्किल हैलाइडों की अभिक्रिया में विलोपन, प्रतिस्पर्धा में प्रतिस्थापन से आगे होता है। यदि तृतीयक एेल्किल हैलाइड का उपयोग किया जाए तो उत्पाद के रूप में केवल एेल्कीन प्राप्त होती है एवं कोई ईथर नहीं बनती। उदाहरणार्थ; CH3ONa की (CH3)3C–Br के साथ अभिक्रिया द्वारा केवल 2-मेथिलप्रोपीन प्राप्त होती है।
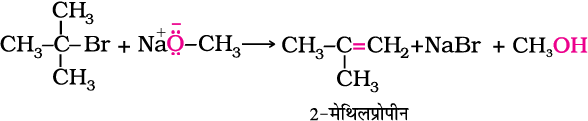
एेसा इसलिए होता है क्योंकि एेल्कॉक्साइड न केवल नाभिकरागी होते हैं अपितु प्रबल क्षारक भी होते हैं। वे एेल्किल हैलाइडों के साथ विलोपन अभिक्रिया करते हैं।
उदाहरण 11.6
निम्नलिखित अभिक्रिया तृतीयक ब्यूटिल एथिल ईथर बनाने के लिए उपयुक्त नहीं है।

(I) इस अभिक्रिया का मुख्य उत्पाद क्या होगा?
(ii) तृतीयक-ब्यूटिलएथिल ईथर बनाने के लिए उपयुक्त अभिक्रिया लिखिए?
हल
(i) दी गई अभिक्रिया में 2-मेथिलप्रोप-1-ईन मुख्य उत्पाद है_ क्योंकि सोडियम एथॉक्साइड एक प्रबल नाभिकरागी एवं प्रबल क्षारक है, अतः विलोपन प्रतिस्थापन से अधिक प्रधान होता है।
(ii) 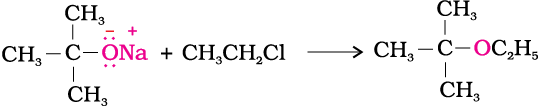
इस विधि सेफ़ीनॉलों को भी ईथरों में परिवर्तित किया जाता है। इसमें फ़ीनॉल का उपयोगफ़ीनाक्सॉइड अर्धांश (Moiety) के रूप में होता है।

11.6.2 भौतिक गुणधर्म
ईथर में C-O आबंध ध्रुवीय होते हैं, अतः ईथरों का नेट द्विध्रुव आघूर्ण होता है। ईथरों की अल्प ध्रुवता उनके क्वथनांकों को बहुत अधिक प्रभावित नहीं करती, जो कि समतुल्य आण्विक द्रव्यमान वाले एेल्केनों के क्वथनांकों के समान होते हैं, परंतु वे एेल्कोहॉलों के क्वथनांकों से बहुत कम होते हैं, जैसा कि निम्नलिखित स्थितियों में दर्शाया गया है–
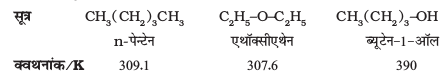
एेल्कोहॉलों एवं ईथरों के क्वथनांकों में अधिक अंतर का कारण एेल्कोहॉलों में हाइड्रोजन आबंधों की उपस्थिति है।
ईथरों की जल में मिश्रणीयता, समान आण्विक द्रव्यमान वाले एेल्कोहॉलों से सदृश्य होती है। एथॉक्सीएथेन एवं ब्यूटेन-1-अॉल दोनों ही जल में लगभग समान रूप से मिश्रणीय होते हैं अर्थात् 100 mL जल में क्रमशः 7.5 g तथा 9 g है जबकि पेन्टेन जल में अमिश्रणीय है। क्या आप इस प्रेक्षण को समझा सकते हैं? इसका कारण यह है कि एेल्कोहॉलों की भाँति ईथरों का अॉक्सीजन परमाणु भी जल के साथ हाइड्रोजन आबंध बनाता है; जैसा कि चित्र में दर्शाया गया है।
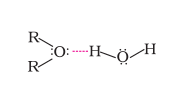
1. ईथरों में C–O आबंध का विदलन
ईथर प्रकार्यात्मक समूहों में सबसे कम अभिक्रियाशील होती हैं। ईथरों केC–O आबंध का विदलन उग्र परिस्थितियों में हाइड्रोजन हैलाइडों के आधिक्य में होता है। डाइएेल्किल ईथर की अभिक्रिया से एेल्किल हैलाइड के दो अणु प्राप्त होते हैं।
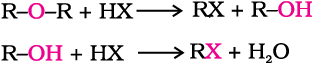
11.6.3 रासायनिक अभिक्रियाएँ
एेरिल-अॉक्सीजन आबंध के अधिक स्थायी होने के कारण एेल्किल एेरिल ईथर का एेल्किल-अॉक्सीजन आबंध विदलित होता है। इस अभिक्रिया सेफ़ीनॉल एवं एेल्किल हैलाइड प्राप्त होते हैं।
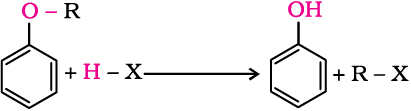
दो विभिन्न एेल्किल समूहों वाली ईथर भी इसी प्रकार से विदलित होती हैं।
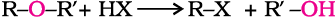
हाइड्रोजन हैलाइडों की अभिक्रियाशीलता का क्रम इस प्रकार होता है–
HI > HBr > HCl ईथरों का विदलन सांद्र HI अथवा HBr द्वारा उच्च ताप पर होता है।
जब इनमें से एक एेल्किल समूह तृतीयक समूह होता है, तो तृतीयक हैलाइड प्राप्त होते हैं।
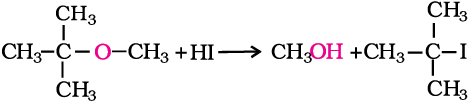
क्रियाविधि
ईथर की सांद्र HI के साथ अभिक्रिया, ईथर के अणु के प्रोटॉनन से प्रारंभ होती है।
चरण–1
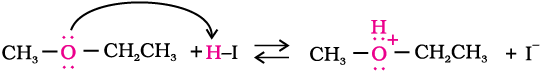
अभिक्रिया HI या HBr के साथ होती है; क्योंकि ये अभिकर्मक पर्याप्त अम्लीय होते हैं।
चरण–2
आयोडाइड एक अच्छा नाभिकरागी है। यह पद 1 से प्राप्त अॉक्सोनियम आयन के अल्पतम प्रतिस्थापित कार्बन पर आक्रमण करता है और SN2क्रियाविधि से एेल्कोहॉल अणु को विस्थापित कर देता है।
अतः दो भिन्न एेल्किल समूह युक्त मिश्रित ईथर के विदलन से बनने वाली एेल्कोहॉल तथा एेल्किल आयोडाइड कौन से होंगे यह एेल्किल समूहों की प्रकृति पर निर्भर करता है। जब प्राथमिक अथवा द्वितीयक एेल्किल समूह उपस्थित होते हैं तो निम्नतर एेल्किल समूह एेल्किल आयोडाइड (SN2 अभिक्रिया) बनते हैं।
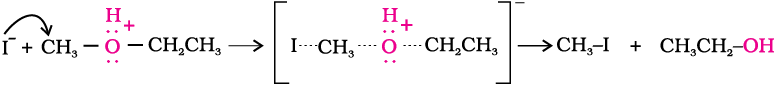
जब HI आधिक्य में होता है और अभिक्रिया उच्च ताप पर की जाती है तो एथेनॉल, HI के दूसरे अणु के साथ अभिक्रिया करके एथिल आयोडाइड में परिवर्तित हो जाती है।
चरण–3
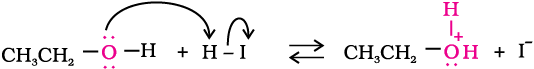

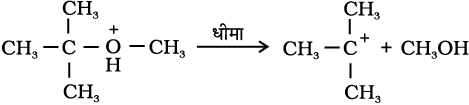
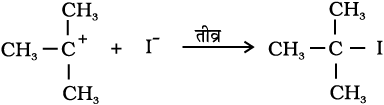
एेनिसोल में ईथर के प्रोटॉनन द्वारा मेथिलफेनिल अॉक्सोनियम आयन 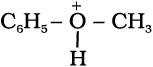
बनता है। फेनिल समूह के कार्बन की sp2 संकरण अवस्था तथा (O–C6H5) समूह के आंशिक द्विआबंध अभिलक्षण के कारण O–CH3 का आबंध O–C6H5 आबंध की तुलना में दुर्बल होता है। इसलिए I– आयन का आक्रमण O–CH3 आबंध को तोड़कर CH3I बनाता है।फ़ीनॉल पुनः अभिक्रिया करके हैलाइड नहीं देते क्योंकिफ़ीनॉल का sp2 संकरित कार्बन (नाभिकरागी) प्रतिस्थापन अभिक्रिया नहीं दर्शा सकता जो कि हैलाइड में परिवर्तन के लिए आवश्यक है।
उदाहरण 11.7 निम्नलिखित ईथरों को HI के साथ गरम करने से प्राप्त मुख्य उत्पाद दीजिए।
(i) 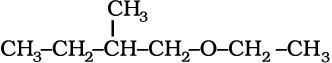
(ii) 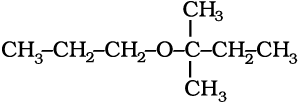
(iii) 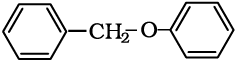
हल
(i) 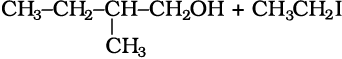
(ii) 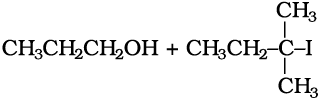
(iii) 
2. इलेक्ट्रॉनरागी प्रतिस्थापन
एेल्कॉक्सी समूह (–OR) अॉर्थो एवं पैरा निर्देशक होता है तथा यहफ़ीनॉल के –OH समूह के समान ही एेरोमैटिक वलय को इलेक्ट्रॉनरागी प्रतिस्थापन के प्रति सक्रिय करता है।

(i) हैलोजनन—
फ़ेनिलएेल्किल ईथर, बेन्जीन वलय में सामान्य हैलोजनन अभिक्रियाएं देता है। उदाहरणार्थ; एेनिसोल का ब्रोमीनन, एथेनॉइक अम्ल में घुली ब्रोमीन द्वारा, आयरन (III) ब्रोमाइड उत्प्रेरक की अनुपस्थिति में भी होता है। एेसा मेथॉक्सी समूह द्वारा बेन्जीन वलय के सक्रिमण के कारण होता है। इसमें पैरा समावयवी की लब्धि 90% होती है।
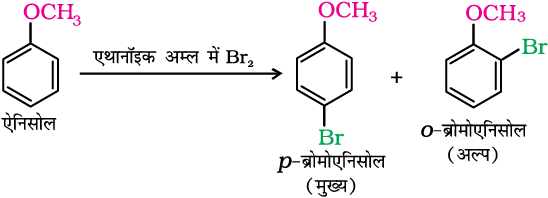
(ii) फ्रीडेल क्राफ्ट अभिक्रिया—
एेनिसोल फ्रीडेल-क्राफ्ट अभिक्रिया देता है एेलुमीनियम क्लोराइड (एक लुईस अम्ल) उत्प्रेरक की उपस्थिति में एेल्किल हैलाइड तथा एेसिल हैलाइड की अभिक्रिया द्वारा एेल्किल तथा एेसिल समूह अॉर्थो तथा पैरा स्थितियों पर प्रवेश करते हैं।
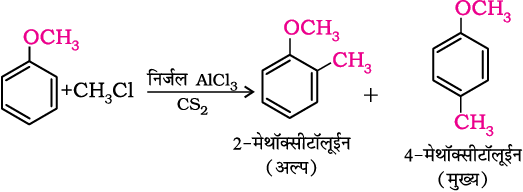
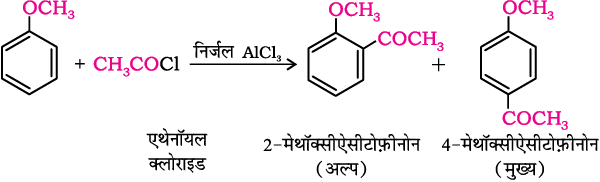
(iii) नाइट्रोकरण—
एेनिसोल, सांद्र H2SO4 और सांद्र HNO3 के मिश्रण के साथ अभिक्रिया द्वारा अॉर्थो और पैरा नाइट्रोएनिसोल का मिश्रण देता है।

पाठ्यनिहित प्रश्न
11.10 एथेनॉल एवं 3-मेथिलपेन्टेन-2-अॉल से प्रारंभ कर 2-एथॉक्सी-3-मेथिलपेन्टेन के विलयम्सन संश्लेषण की अभिक्रिया लिखिए।
11.11 1-मेथॉक्सी-4-नाइट्रोबेन्जीन के विरचन के लिए निम्नलिखित अभिकारकों में से कौन सा युग्म उपयुक्त है और क्यों?
(i) 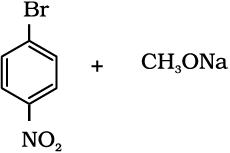 (ii)
(ii) 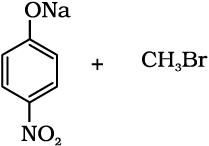
11.12 निम्नलिखित अभिक्रियाओं से प्राप्त उत्पादों का अनुमान लगाइए–
(i) 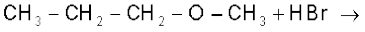 (ii)
(ii) 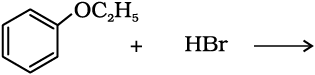
(iii) 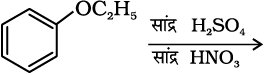 (iv)
(iv) 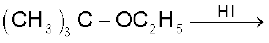
सारांश
एेल्कोहॉलों एवं फ़ीनॉलों का वर्गीकरण– (i) हाइड्रॉक्सिल समूहों की संख्या व (ii) कार्बन परमाणु के sp3 या sp2 संकरण जिससे कि –OHसमूह जुड़ा होता है, के आधार पर किया जाता है। ईथरों का वर्गीकरण अॉक्सीजन परमाणु से जुड़े समूहों के आधार पर किया जाता है।
एेल्कोहॉलों को निम्नलिखित विधियों द्वारा बनाया जा सकता है–
(1) एेल्कीनों के जलयोजन से– (i) अम्ल की उपस्थिति में तथा (ii)हाइड्रोबोरॉनन-आक्सीकरण अभिक्रिया द्वारा
(2) कार्बोनिल यौगिकों से– (i) उत्प्रेरकी अपयचन तथा (ii) ग्रीन्यार अभिकर्मक की क्रिया द्वारा
फ़ीनॉलों को निम्नलिखित विधियों द्वारा बनाया जा सकता है–
(1) –OH समूह से प्रतिस्थापन द्वारा– (i) हैलोएेरीन में हैलोजन परमाणु का तथा (ii) एेरिल सल्फोनिक अम्ल में सल्फोनिक अम्ल समूह का प्रतिस्थापन।
(2) डाइएेज़ोनियम लवणों के जलअपघटन द्वारा।
(3) क्यूमीन से औद्योगिक उत्पादन द्वारा।
लगभग तुल्य द्रव्यमान वाले अन्य वर्गों, जैसे- हाइड्रोकार्बनों, ईथरों तथाहैलोएेल्केनों के यौगिकों की तुलना में एेल्कोहॉलों के क्वथनांक अधिकहोते हैं। एेल्कोहॉलों,फ़ीनॉलों एवं ईथरों की जल के साथ अंतराआण्विकहाइड्रोजन आबंध बनाने की क्षमता के कारण यह जल में घुलनशील होती हैं।
एेल्कोहॉल एवंफ़ीनॉल अम्लीय प्रकृति की होती हैं।फ़ीनॉलों में इलेक्ट्रॉन अपनयक समूह इनकी अम्ल प्रबलता को बढ़ाते हैं तथा इलेक्ट्रॉन दाता (विमोचक) समूह अम्ल प्रबलता को कम करते हैं।
एेल्कोहॉल हाइड्रोजन हैलाइडों के साथ नाभिकरागी प्रतिस्थापन द्वारा एेल्किल हैलाइड प्रदान करते हैं। एेल्कोहॉलों का निर्जलन एेल्कीन देता है। दुर्बल अॉक्सीकारकों द्वारा प्राथमिक एेल्कोहॉल अॉक्सीकृत होकरएेल्डिहाइड प्रदान करते हैं तथा प्रबल अॉक्सीकारकों द्वारा कार्बोक्सिलिकअम्ल प्राप्त होते हैं। जबकि द्वितीयक एेल्कोहॉल कीटोन देते हैं। तृतीयक एेल्कोहॉल अॉक्सीकरण प्रतिरोधी होते हैं।
फ़ीनॉलों में, –OH समूह की उपस्थिति, एेरोमैटिक वलय कोइलेक्ट्रॉनरागी प्रतिस्थापन के प्रति सक्रियित कर देती है एवं अनुनादीप्रभाव के कारण आने वाले समूह को अॉर्थो तथा पैरा स्थितियों की ओर निर्दिष्ट करती है।फ़ीनॉल की राइमर-टीमन अभिक्रिया सैलिसैल्डिहाइड प्रदान करती है। सोडियम हाइड्राक्साइड की उपस्थिति मेंफ़ीनॉलफ़ीनॉक्साइड आयन देता है जोफ़ीनॉल से अधिक क्रियाशील होता है अतः क्षारीय माध्यम मेंफ़ीनॉल कोल्बे अभिक्रिया देती है।
ईथरों को– (i) एेल्कोहॉलों के निर्जलन तथा (ii) विलियम्सन संश्लेषणविधि द्वारा बनाया जाता है।
ईथरों के क्वथनांक एेल्केनों से मिलते-जुलते होते हैं। जबकि इनकी विलेयता समान आण्विक द्रव्यमान वाले एेल्कोहॉलों से तुल्य होती हैं। ईथरों के C–O आबंध को हाइड्रोजन हैलाइडों द्वारा विदलित किया जा सकता है। इलेक्ट्रॉनरागी प्रतिस्थापन में, एेल्कॉक्सी समूह एेरोमैटिकवलय को सक्रिय बनाता है तथा प्रवेश करने वाले समूह को अॉर्थो एवंपैरा स्थितियों की ओर निर्दिष्ट करता है।
अभ्यास
11.1 निम्नलिखित यौगिकों के आईयूपीएसी (IUPAC) नाम लिखिए।
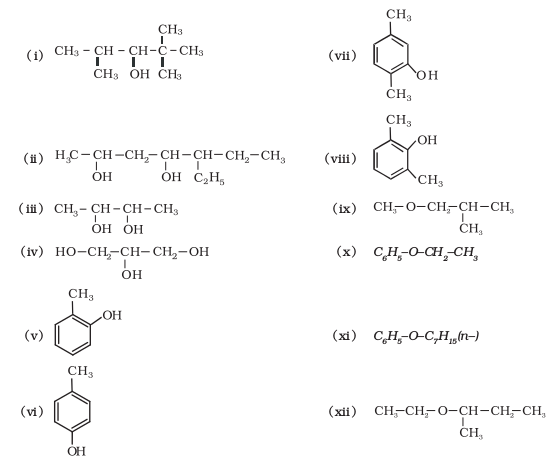
11.2 निम्नलिखित आईयूपीएसी (IUPAC) नाम वाले यौगिकों की संरचनाएं लिखिए–
(i) 2-मेथिलब्यूटेन -2-अॉल (vi) 2-एथॉक्सी-3-मेथिलपेन्टेन
(ii) 1-फ़ेनिलप्रोपेन-2-अॉल (vii) साइक्लोहैक्सिलमेथेनॉल
(iii) 3, 5-डाइमेथिलहैक्सेन-1,3,5,-ट्राइअॉल
(viii) 3-साइक्लोहैक्सिलपेन्टेन-3-अॉल
(iv) 2, 3-डाइएथिलफ़ीनॉल (ix) साइक्लोपेन्टेन-3-ईन-1-अॉल
(v) 1-एथॉक्सीप्रोपेन (x) 4-क्लोरो-3-एथिलब्यूटेन-1-अॉल
11.3 (i) C5H12O आण्विक सूत्र वाले एेल्कोहॉलों के सभी समावयवों की संरचना लिखिए एवं उनके आईयूपीएसी (IUPAC) नाम दीजिए।
(ii) प्रश्न 11.3 (i) के समावयवी एेल्कोहॉलों को प्राथमिक, द्वितीयक एवं तृतीयक एेल्कोहॉलों में वर्गीकृत कीजिए।
11.4 समझाइए कि प्रोपेनॉल का क्वथनांक, हाइड्रोकार्बन ब्यूटेन से अधिक क्यों होता है?
11.5 समतुल्य आण्विक भार वाले हाइड्रोकार्बनों की अपेक्षा एेल्कोहॉल जल में अधिक विलेय होते हैं इस तथ्य को समझाइए।
11.6 हाइड्रोबोरॉनन-अॉक्सीकरण अभिक्रिया से आप क्या समझते हैं? इसे उदाहरण सहित समझाइए।
11.7 आण्विक सूत्र C7H8O वाले मोनोहाइड्रिकफ़ीनॉलों की संरचनाएं तथा आईयूपीएसी (IUPAC) नाम लिखिए।
11.8 अॉर्थो तथा पैरा-नाइट्रोफ़ीनॉलों के मिश्रण को भाप-आसवन द्वारा पृथक् करने में भाप-वाष्पशील समावयवी का नाम बताइए। इसका कारण दीजिए।
11.9 क्यूमीन सेफ़ीनॉल बनाने की अभिक्रिया का समीकरण दीजिए।
11.10 क्लोरोबेन्जीन सेफ़ीनॉल बनाने की रासायनिक अभिक्रिया लिखिए।
11.11 एथीन के जलयोजन से एथेनॉल प्राप्त करने की क्रियाविधि लिखिए।
11.12 आपको बेन्जीन, सांद्र H2SO4 और NaOH दिए गए हैं। इन अभिकर्मकों के उपयोग द्वाराफ़ीनॉल के विरचन की समीकरण लिखिए।
11.13 आप निम्नलिखित को कैसे संश्लेषित करेंगे? दर्शाइए।
(i) एक उपयुक्त एेल्कीन से 1-फ़ेनिलएथेनॉल
(ii) SN2 अभिक्रिया द्वारा एेल्किल हैलाइड के उपयोग से साइक्लोहेक्सिलमेथेनॉल
(iii) एक उपयुक्त एेल्किल हैलाइड के उपयोग से पेन्टेन-1-अॉल
11.14 एेसी दो अभिक्रियाएं दीजिए जिनसेफ़ीनॉल की अम्लीय प्रकृति प्रदर्शित होती हो,फ़ीनाल की अम्लता की तुलना एथेनॉल से कीजिए।
11.15 समझाइए कि अॉर्थो-नाइट्रोफ़ीनॉल, अॉर्थो-मेथॉक्सीफ़ीनॉल से अधिक अम्लीय क्यों होती है?
11.16 समझाइए कि बेन्जीन वलय से जुड़ा –OH समूह उसे इलेक्ट्रॉनरागी प्रतिस्थापन के प्रति कैसे सक्रियित करता है?
11.17 निम्नलिखित अभिक्रियाओं के लिए समीकरण दीजिए–
(i) प्रोपेन-1-अॉल का क्षारीय KMnO4 के साथ अॉक्सीकरण
(ii) ब्रोमीन की CS2 मेंफ़ीनॉल के साथ अभिक्रिया (iii) तनु HNO3 कीफ़ीनॉल से अभिक्रिया
(iv) फ़ीनॉल की जलीय NaOH की उपस्थिति में क्लोरोफार्म के साथ अभिक्रिया
11.18 निम्नलिखित को उदाहरण सहित समझाइए—
(i) कोल्बे अभिक्रिया (ii) राइमर-टीमन अभिक्रिया (iii) विलियम्सन ईथर संश्लेषण (iv) असममित ईथर।
11.19 एथेनॉल के अम्लीय निर्जलन से एथीन प्राप्त करने की क्रियाविधि लिखिए।
11.20 निम्नलिखित परिवर्तनों को किस प्रकार किया जा सकता है?
(i) प्रोपीन → प्रापेन-2-अॉल (iii) एथिल मैग्नीशियम क्लोराइड → प्रापेन-1-अॉल
(ii) बेन्जिल क्लोराइड → बेन्जिल एेल्कोहॉल (iv) मेथिल मैग्नीशियम ब्रोमाइड → 2-मेथिलप्रोपेन-2-अॉल
11.21 निम्नलिखित अभिक्रियाओं में प्रयुक्त अभिकर्मकों के नाम बताइए—
(i) प्राथमिक एेल्कोहॉल का कार्बोक्सिलिक अम्ल में आक्सीकरण (iv) बेन्जिल एेल्कोहॉल से बेन्ज़ोइक अम्ल
(ii) प्राथमिक एेल्कोहॉल का एेल्डिहाइड में आक्सीकरण (v) प्रोपेन-2-अॉल का प्रोपीन में निर्जलन
(iii) फ़ीनॉल का 2,4,6-ट्राइब्रोमोफीनॉल में ब्रोमीनन (vi) ब्यूटेन-2-अॉन से ब्यूटेन-2-अॉल
11.22 कारण बताइए कि मेथॉक्सीमेथेन की तुलना में एथेनॉल का क्वथनांक उच्च क्यों होता है?
11.23 निम्नलिखित ईथरों के आईयूपीएसी (IUPAC) नाम दीजिए—
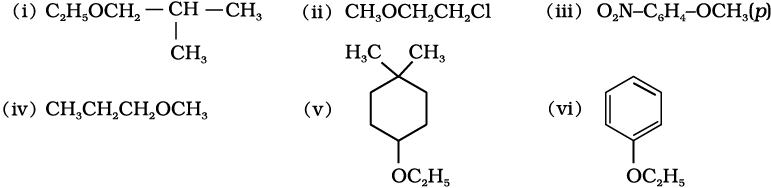
11.24 निम्नलिखित ईथरों को विलियम्सन संश्लेषण द्वारा बनाने के लिए अभिकर्मकों के नाम एवं समीकरण लिखिए—
(i) 1-प्रोपॉक्सीप्रोपेन (ii) एथॉक्सीबेन्जीन (iii) 2-मेथॉक्सी-2-मेथिलप्रोपेन (iv) 1-मेथॉक्सीएथेन
11.25 कुछ विशेष प्रकार के ईथरों को विलियम्सन संश्लेषण द्वारा बनाने की सीमाओं को उदाहरणों से समझाइए।
11.26 प्रोपेन-1-अॉल से 1-प्रोपाक्सीप्रोपेन को किस प्रकार बनाया जाता है? इस अभिक्रिया की क्रियाविधि लिखिए।
11.27 द्वितीयक अथवा तृतीयक एेल्कोहॉलों के अम्लीय निर्जलन द्वारा ईथरों को बनाने की विधि उपयुक्त नहीं है। कारण बताइए।
11.28 हाइड्रोजन आयोडाइड की निम्नलिखित के साथ अभिक्रिया के लिए समीकरण लिखिए–
(i) 1-प्रोपॉक्सीप्रोपेन (ii) मेथॉक्सीबेन्जीन तथा (iii) बेन्ज़िल एथिल ईथर
11.29 एेरिल एेल्किल ईथरों में निम्न तथ्यों की व्याख्या कीजिए–
(i) एेल्कॉक्सी समूह बेन्जीन वलय को इलेक्ट्रॉनरागी प्रतिस्थापन के प्रति सक्रियित करता है, तथा
(ii) यह प्रवेश करने वाले प्रतिस्थापियों को बेन्जीन वलय की अॉर्थो एवं पैरा स्थितियों की ओर निर्दिष्ट करता है।
11.30 मेथॉक्सीमेथेन की HI के साथ अभिक्रिया की क्रियाविधि लिखिए।
11.31 निम्नलिखित अभिक्रियाओं के लिए समीकरण लिखिए–
(i) फ्रीडेल-क्राफ्ट अभिक्रिया–एेनिसोल का एेल्किलन (iii) एथेनॉइक अम्ल माध्यम में एेनिसोल का ब्रोमीनन
(ii) एेनिसोल का नाइट्रोकरण (iv) एेनिसोल का फ्रीडेल-क्राफ्ट एेसीटिलन।
11.32 उपयुक्त एेल्कीनों से आप निम्नलिखित एेल्कोहॉलों का संश्लेषण कैसे करेंगे?
(i) 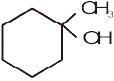 (ii)
(ii) 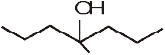 (iii)
(iii) 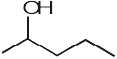 (iv)
(iv) 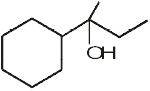
11.33 3-मेथिलब्यूटेन-2-अॉल को HBr से अभिकृत कराने पर निम्नलिखित अभिक्रिया होती है—

इस अभिक्रिया की क्रियाविधि दीजिए।
(संकेत– चरण II में प्राप्त द्वितीयक कार्बोकैटायन हाइड्राइड आयन विचलन के कारण पुनर्विन्यासित होकर स्थायी तृतीयक कार्बोकैटायन बनाते हैं।)
कुछ पाठ्यनिहित प्रश्नों के उत्तर
11.1 प्राथमिक एेल्कोहॉल (i) (ii) (iii)
द्वितीयक एेल्कोहॉल (iv) तथा (v)
तृतीयक एेल्कोहॉल (vi)
11.2 एेलिलिक एेल्कोहॉल (ii) तथा (vi)
11.3 (i) 4-क्लोरो-3-एथिल-2-(1-मेथिल एथिल)-ब्यूटेन-1-अॉल (iv) हेक्स-1-ईन-3-अॉल
(ii) 2, 5-डाइमेथिलहेक्सेन-1,3-डाइअॉल (v) 2-ब्रोमो-3-मेथिलब्यूट-2-ईन-1-अॉल
(iii) 3-ब्रोमोसाइक्लोहेक्सेनअॉल
11.4 (i) 
(ii) 
11.5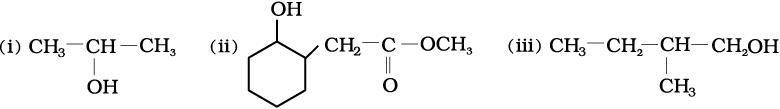
11.7 (i) 1-मेथिलसाइक्लोहेक्सीन (ii) ब्यूट-1-ईन एवं ब्यूट-2-ईन का मिश्रण बनता है जिसमें ब्यूट-2-ईन मुख्य उत्पाद होती है क्योंकि पुनर्विन्यास द्वारा सेकेंड्री कार्बोकैटायन बनता है।
11.10 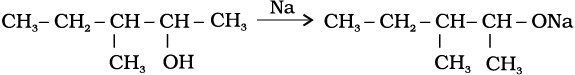
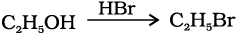
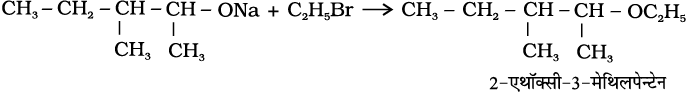
11.11 (ii) 11.12 (i) 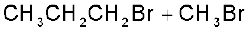 (ii)
(ii) 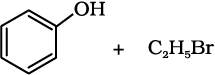
(iii) 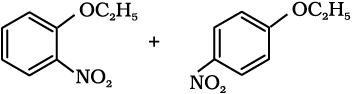 (iv)
(iv)